藥花香里說豐年,聽取me-too一片

【新聞事件】:今天著名生物技術投資人Bruce Booth發(fā)表博文回顧2017年制藥行業(yè)成績。盡管今年還剩一個月,但是FDA已經(jīng)批準了40個新分子藥物和2個CAR-T細胞療法。鑒于12月是批準高峰月,今年很可能打破2015年45個的新藥記錄(除了情況特殊的1996年)。但是Booth也注意到今年批準的藥物只有19%是首創(chuàng)藥物,不僅遠低于2012年的51%,而且過去5年似乎在呈下降趨勢(見下圖)。他說如果這是一個真實的趨勢,那么會對行業(yè)產(chǎn)生一定影響,如首創(chuàng)獨占市場時間下降、對臨床開發(fā)依賴增強(以做出區(qū)分)、誘發(fā)價格戰(zhàn)等。
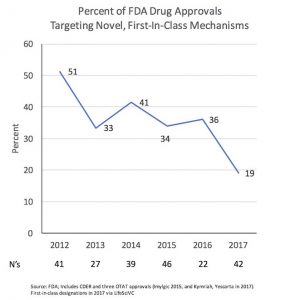
【藥源解析】:首先今天是個豐收年是沒有什么疑問了。今年45個左右新藥遠遠高于去年的22個,也接近歷史記錄,可喜可賀。至于me-too藥物是否過多我看是有點多慮了,如果那條曲線真是一個真實趨勢那么倒推到90年代就沒什么me-too藥物了。但我清晰記得21世紀初每年只有5個左右首創(chuàng)藥物的時代,有一年只有兩個首創(chuàng)藥物。2006年統(tǒng)計當時有1357個藥物,但只有324個靶點,不用計算器也能大概看出以前me-too藥物也是絕對主流。
但現(xiàn)在這些me-too和古代的me-too是不同的。以前那是真叫me-too,十幾個beta阻斷劑上市了還有人剛剛開始做新的beta-阻斷劑。現(xiàn)在也有人微調(diào)大環(huán)內(nèi)酯、四環(huán)素,但多數(shù)是幾乎同時開始的項目。只是上市有先后,比賽必須有人輸。另外一個造成多個同類藥物前后腳上市的因素是現(xiàn)在新藥競爭決勝路段通常是在臨床開發(fā)階段。很多藥物進入臨床但不一定全速開發(fā),一旦有人做出概念驗證會立即有本來搖擺不定的項目跟上。因為臨床開發(fā)時間相對較短,更容易造成同類藥物一兩年內(nèi)先后上市的現(xiàn)象。PARP和CDK4/6抑制劑是非常明顯的例子。當然也有PCSK9這種全程高速競爭的例子,但不如以前多。
多數(shù)上市藥物是me-too也不等于制藥工業(yè)不思進取,也不等于me-too是個主流模式。事實上前一陣福泰的科學家分析顯示現(xiàn)在70%以上疾病-機理組合只有一個項目在探索,只是me-too藥物成功率較高所以在上市藥物中富集了。雖然me-too藥物成功率明顯高于首創(chuàng),但商業(yè)回報通常低于首創(chuàng),尤其在已經(jīng)有不止一個藥物上市的市場。即使PD-1這樣多年不遇的靶點第4、5個上市、僅落后2-3年的me-too藥物也很難參與競爭,經(jīng)常被迫在危險路段彎道超車,日子并不好過。
★更多深度解析訪問《美中藥源》~
★ 請關注《美中藥源》微信公眾號 ★

發(fā)表評論
要發(fā)表評論,您必須先登錄。


















 微信號:美中藥源
微信號:美中藥源