
靶向exosite提高選擇性:Exo獲7800萬支持
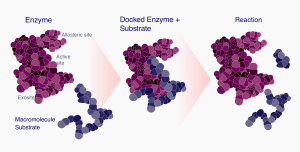
【新聞事件】:今天美國生物技術(shù)公司Exo Therapeutics宣布獲得Nextech Invest 領(lǐng)投的7800萬美元B輪支持,令其總?cè)谫Y額達(dá)到一億美元。Exo的技術(shù)平臺是阻斷酶底物與酶的結(jié)合位點(exosite)、叫ExoSight。這區(qū)別于傳統(tǒng)的活性腔抑制劑或間接調(diào)節(jié)活性腔活性的別構(gòu)抑制劑。Exo起源于2014年哈佛大學(xué)David Liu實驗室對胰島素降解蛋白(IDE)的研究,但現(xiàn)在Exo并沒有開發(fā)IDE抑制劑,而是有四個項目靶向腫瘤、抗炎兩大疾病。
【藥源解析】:小分子藥物與其它新技術(shù)比的一個重要缺陷就是選擇性相對較差,導(dǎo)致脫靶毒性成為小分子藥物開發(fā)的一個嚴(yán)重障礙。小分子藥物選擇性比較差的原因有幾個。一是活性腔抑制劑通常分子較小、因此特異性較差,如同較短密碼更容易撞衫。二是很多酶有結(jié)構(gòu)類似但功能不同的同源蛋白,令這些小分子難以區(qū)分這些長得高度相似的活性腔、誤傷其它生命過程。三是IDE這種多功能酶。IDE不僅降解胰島素、同時還降解glucagon,如果關(guān)閉催化活性,胰島素雖然水平會上升但glucagon也同樣會水平升高,結(jié)果殺敵一千、自損八百,血糖控制沒有改善。
David Liu的2014年《自然》文章靶向IDE與胰島素的結(jié)合,而不是IDE活性腔。酶要催化化學(xué)反應(yīng)首先要與底物結(jié)合,所以阻斷這個過程也同樣可以抑制酶反應(yīng)。這個思路可以保留酶的活性,但干擾某個特定底物與多功能酶的結(jié)合、所以提高選擇性。Exosite雖然不是活性腔,但與別構(gòu)結(jié)合腔還是有區(qū)別的。別構(gòu)腔抑制劑間接干擾活性腔的構(gòu)象,所以還是會干擾酶對所有底物的催化。別構(gòu)抑制劑有時可以提高對同源蛋白的選擇性,但exosite抑制劑提高的多功能酶對不同底物的選擇性。比如他們當(dāng)年發(fā)現(xiàn)的抑制劑不干擾IDE與glucagon的結(jié)合。
很多酶的底物是另一個蛋白,制藥業(yè)主流靶點家族如激酶、蛋白酶、磷酸酶等都是對蛋白的修飾。所以雖然干擾底物與酶結(jié)合是個顯而易見的思路但技術(shù)上并不容易,因為這通常要求你阻斷蛋白蛋白相互作用(PPI)。雖然PPI過去幾年有了較大進(jìn)展,尤其是BCL、MCL等調(diào)控細(xì)胞凋亡的關(guān)鍵蛋白有了可成藥抑制劑,但總的來說成藥性較差。一個關(guān)鍵的賦能技術(shù)是DNA編碼化合物庫(DEL)。PPI的結(jié)合區(qū)通常較大、但沒有什么高強度結(jié)合點,而DEL化合物庫通常也是分子較大、但復(fù)雜性較低,所以二者志趣相投。
DEL兩年前曾經(jīng)紅極一時,但最近兩年被PROTAC搶了風(fēng)頭。Exo老大預(yù)測靶向exosite會和PROTAC一樣成為主流技術(shù),但DEL似乎并沒有達(dá)到當(dāng)年的預(yù)期。David Liu以前曾經(jīng)創(chuàng)建一個DEL為平臺的公司叫做Ensemble,主要靶向IL17與其受體的結(jié)合,但后來無疾而終。DEL最成功的例子是葛蘭素RIPK1抑制劑的發(fā)現(xiàn),遺憾的是這樣高水平的工作并不常見。
美中藥源原創(chuàng)文章,轉(zhuǎn)載注明出處并添加超鏈接,商業(yè)用途需經(jīng)書面授權(quán)。★更多深度解析訪問《美中藥源》~
★ 請關(guān)注《美中藥源》微信公眾號 ★

發(fā)表評論
要發(fā)表評論,您必須先登錄。

















 微信號:美中藥源
微信號:美中藥源