小分子藥物的“小”
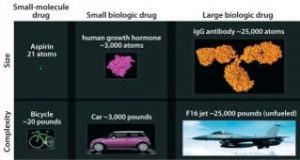
現代制藥工業(yè)開始于小分子藥物,小分子是制藥業(yè)歷史最為悠久的板塊。小分子藥物持續(xù)產出能力令人驚嘆、占所有上市藥物的90%,即使在基因療法、細胞療法、蛋白、RNA藥物大舉進攻的現在小分子藥物仍然是絕對主角,過去5年FDA批準的藥物中70-80%仍然是小分子藥物。小分子藥物生命力如此強大的核心秘密在于“小”字,今天就聊一聊這個話題。
大小分子藥物與靶點的結合能雖然有差別但不大,因此小分子的配體效率(單位分子量貢獻的療效)遠高于其它療法。這個高效率有幾個根本性的后果。一是給藥方式。患者最容易接受的給藥方式是口服,雖然口服藥物性質分布有一定范圍、但還是有個實操上限的。除了小分子藥物外,其它治療板塊(如核酸、蛋白藥物)都無法突破這個分子量上限、所以無法口服,有些大分子連皮下注射都很困難。二是靶點覆蓋范圍,小分子因為身材矮小可以調控胞內、胞外、和游離靶點,而生物大分子就受到一些限制。有些組織如中樞目標必須得靠小分子藥物,如同有些任務只能靠007這樣的孤膽英雄、而不能用一個師的普通士兵。靶點覆蓋范圍廣也令小分子藥物成為最適合表型篩選的板塊,而表型篩選是新藥的一個重要來源。
小分子藥物的另一個優(yōu)勢是對制藥人技術水平比較寬容,在有機化學非常粗糙的時代Hoffmann就曾在11天之內利用乙酰化這個現在看起來非常寒酸的反應發(fā)明了阿司匹林和海洛因這兩個著名藥物,前者到現在還在廣泛應用、后者則因為成癮性而淪為失足藥物。當然隨著技術的發(fā)展小分子藥物設計也越來越復雜,從結構高度復雜的軟海綿素到功能高度復雜的PROTAC、令Hoffmann九泉之下羨慕不已。對技術要求低令小分子藥物起步遠早于生物大分子,這個先發(fā)優(yōu)勢令制藥界積累了大量小分子設計的經驗和知識,比如什么樣的化合物能成藥、什么樣的化合物難成藥現在非常清楚。一個先導物是否有足夠潛力優(yōu)化成藥物、從哪個角度開始優(yōu)化也非常成熟。這些知識為小分子的持續(xù)發(fā)展提供了動力。
小分子藥物因為生產、儲存、運輸比較簡單所以成本和價格也較低,因為易于模仿所以專利過期后價格更是會跌成化工材料價格,這從長期看對整個社會是個有益因素。小分子藥物通常半衰期較短,這雖然令給藥頻率增加但如果出現毒副反應也更容易通過停藥逆轉、事實上避免蓄積是小分子藥物設計的一個指標。小分子因為分子較小所以沒有免疫原性,也少了不少麻煩。
分子量小也有不利的一面,那就是因為太小所以形狀有限、與靶點的結合面積和方式也有限,這造成了小分子藥物選擇性較差。選擇性差最直接的后果是令脫靶毒性成為小分子藥物的一個致命軟肋,三期臨床不結束誰也甭想睡個安穩(wěn)覺、上市之后因為安全性撤市的事情也時有發(fā)生。當然脫靶活性也有有利的一面。首先這令高通量篩選成為可能,一個優(yōu)質化合物庫可以長時間支撐新靶點藥物發(fā)現、吃完被告吃原告。二是脫靶活性為臨床意外發(fā)現提供了空間,比如超重磅藥物Lyrica、Zetia一開始分別是按GABA-AT抑制劑和ACAT抑制劑設計,上市后才發(fā)現分別通過阻斷鈣離子通道、NPC1L1起效。如果這兩個藥物沒有這些脫靶活性我們只能證明GABA-AT、ACAT是錯誤靶點,但因為這些脫靶活性我們得到兩個重要藥物。三是低選擇性也為多靶點藥物提供了機會,比如高選擇性COX2抑制劑的心血管毒性可能是因為COX2/COX1功能失衡。而高選擇性NMDA受體調控劑rapastinel則失去了氯胺酮的抗抑郁療效。
當然“小”只是一個表象,其背后是自然界億萬年演化的血腥歷史。天然產物是物種爭奪生存空間的分子武器、如同人類戰(zhàn)爭用的十八般兵器,都是有故事的精英化合物。一個極端的例子是萬古霉素,可以與細菌細胞壁的d-ala-d-ala這樣一個簡單結構有效結合。假如沒有天然產物、這種反客為主的化合物沒有可能通過人工設計出來,設計出來也沒人會投人資源去合成、驗證。據統(tǒng)計60%的上市藥物是天然產物及其衍生物,所以小分子藥物能成為一路實力強大的諸侯天然產物起了重要作用。前幾年Martin Burke提出一個所謂化學登月計劃,準備利用自動合成技術合成75%的天然產物,這個目標如果能實現一半都是對小分子藥物研發(fā)的巨大推動。
一個分子無論大小要成為藥物需要非常全面的技能,一個小個頭分子能成藥意味著其功能也更強大、所以小分子藥物這個命名沒有準確反映這類藥物的精神氣。Naming is framing,小分子藥物更準確的名字應該叫高效率藥物。
美中藥源原創(chuàng)文章,轉載注明出處并添加超鏈接,商業(yè)用途需經書面授權。★更多深度解析訪問《美中藥源》~
★ 請關注《美中藥源》微信公眾號 ★

發(fā)表評論
要發(fā)表評論,您必須先登錄。


















 微信號:美中藥源
微信號:美中藥源