
ADC到底是什么?(十三)抗體-抗原復(fù)合物誰當(dāng)家?

ADC在腫瘤微環(huán)境中與靶點形成復(fù)合物后發(fā)生什么是ADC設(shè)計需要考慮的重要因素,因為這涉及到哪些微環(huán)境指標(biāo)能預(yù)測藥物應(yīng)答(不一定是抗原高表達喲)這個關(guān)鍵問題。抗原有自己的作息時間、抗體也有自己的生活方式,真實世界中這個復(fù)合物命運如何并非一個簡單問題。當(dāng)前設(shè)計主要關(guān)注抗原的內(nèi)吞和胞內(nèi)轉(zhuǎn)運,但螳螂捕蟬黃雀在后、免疫細(xì)胞介導(dǎo)的ADC降解處理不容忽視。
細(xì)胞生活在水溶液中,蛋白和核酸等核心生物大分子需要被不溶于水脂分子組成的細(xì)胞膜包裹起來。這跟包餃子類似,皮要是溶于水就成片湯了。細(xì)胞膜除了脂雙層骨架還有不少膜蛋白,參與安保、傳播小道消息、快遞生活必需品等功能。偶聯(lián)藥物就是依靠這些膜蛋白的特殊位置和功能將毒素遞送到胞內(nèi),如果表達特異還可以實現(xiàn)選擇性。
膜蛋白在細(xì)胞膜中不是隨機分布的,而是會形成各類功能團體。每個蛋白在膜上保留多少、停留多長時間、遇到什么情況需要離開膜是受到嚴(yán)格監(jiān)管的,因此演化出多種內(nèi)吞機制維持這個動態(tài)平衡。有些受體本來就像擺渡車一樣在膜與胞內(nèi)循環(huán)(constitutive trafficking),有些受體與配體結(jié)合后會改變構(gòu)象(分子的擺拍姿勢)而啟動各種內(nèi)吞機制,這兩種情況配體在膜上搭上順風(fēng)車都可以進到胞內(nèi)。也有一些受體內(nèi)吞能力很差,ADC靶向這類靶點需要設(shè)計對應(yīng)的鏈接子斷裂方式。
但抗體并不是總能將就抗原的生活方式。抗體作為獲得性免疫系統(tǒng)的重要組成部分有時人在江湖身不由己,與免疫細(xì)胞合作清除外源性病原體是首要任務(wù)、而不是跟著抗原去胞內(nèi)閑逛。病原體以生物大分子為核心,從化學(xué)角度看免疫系統(tǒng)的主要功能是降解這些生物大分子,比如細(xì)菌用的CRISPR系統(tǒng)。高級生物免疫系統(tǒng)更高級,降解前可能會先做一些準(zhǔn)備工作如破壞病原體外包裝等。抗體是一類多功能分子,包含能準(zhǔn)確識別敵人的可變區(qū)和調(diào)動生命體武裝力量、降解這些有害物質(zhì)的恒定區(qū),介導(dǎo)ADCC、ADCP、CDC效應(yīng)。
抗體在江湖上以選擇性高而聞名,但是抗體從人海中找到敵人后還需要利用各種免疫細(xì)胞完成安全銷戶。對ADC藥物來說抗體將抗原交給哪類免疫細(xì)胞、能不能及時聯(lián)系上免疫細(xì)胞涉及到整個復(fù)合物誰當(dāng)家的問題,抗原內(nèi)化與抗體介導(dǎo)免疫效應(yīng)的相對速率決定毒素在哪里釋放、什么樣的微環(huán)境釋放毒素效率更高。通常ADC候選藥物會在體外實驗中測一下內(nèi)吞效率,抗體介導(dǎo)的ADCC、ADCP等免疫效應(yīng)也是很明確的,但在復(fù)雜的腫瘤微環(huán)境中這兩類過程的相對動力學(xué)卻難以評價。
不僅這方面數(shù)據(jù)很少,而且可以想象每個抗體-抗原復(fù)合物的命運會與抗原內(nèi)在調(diào)控機制、抗原密度、結(jié)合位點、結(jié)合強度、抗體Fc功能、微環(huán)境里面免疫細(xì)胞組成和免疫抑制程度等多種因素有關(guān)。毒素在哪里、以多快速度釋放還與FcRn回收、組織蛋白酶活性、胞內(nèi)轉(zhuǎn)運效率等更多因素有關(guān),而最終ADC的療效和安全性還要受毒素進出細(xì)胞膜速度、在微環(huán)境里面穿行速度、自身治療窗口等因素有關(guān)。說ADC是一類復(fù)雜藥物都有點天涼好個秋的味道了。
以研究最充分的HER2為例,這個最成功的ADC靶點到現(xiàn)在還有一些不解之謎。膜上HER2受體不僅自己很難下調(diào),而且其它膜受體與其二聚后內(nèi)化也會受到抑制。HER2沒有天然配體,抗體是HER2第一次見到的胞外來客,經(jīng)常表現(xiàn)的手足無措。不同表位的HER2抗體是否能誘導(dǎo)HER2內(nèi)化數(shù)據(jù)比較混亂,沒有公認(rèn)結(jié)論。早期研究顯示HER2抗體內(nèi)化效率非常低,但后來發(fā)現(xiàn)膜上HER2密度較低時與抗體結(jié)合可以內(nèi)吞、并可以到達溶酶體降解,但高密度時不僅內(nèi)吞慢、而且內(nèi)吞后會很快被回收到膜上。
從抗體角度看抗原密度越高、形成復(fù)合物后就越容易被免疫細(xì)胞識別、摧毀、和吞噬。免疫細(xì)胞可能通過ADCP等效應(yīng)把ADC連帶腫瘤細(xì)胞一并內(nèi)吞和降解,成為介導(dǎo)旁觀者殺傷的一個機制。也可以通過ADCC效應(yīng)比ADC快一步破壞腫瘤細(xì)胞,失去毒素釋放環(huán)境。目前ADC主要用于單抗藥物耐藥后的二線場景、所以單憑免疫效應(yīng)可能已經(jīng)不足以控制腫瘤增長了。T-DM1在一線場景并未超過單抗與化療組合,T-DXd的一線臨床正在進行中、早期應(yīng)答率數(shù)據(jù)看至少與單抗化療標(biāo)準(zhǔn)療法類似。
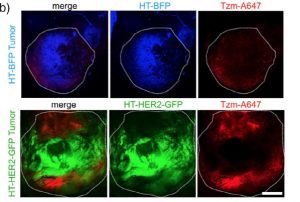
我們很難知道抗體與抗原結(jié)合后先被標(biāo)記細(xì)胞內(nèi)吞,還是先通知免疫系統(tǒng)摧毀或吞飲標(biāo)記過的細(xì)胞。幾年前哈佛的科學(xué)家發(fā)現(xiàn)曲妥珠(下圖紅色)在小鼠模型中HER2陽性腫瘤(綠色)比HER2陰性腫瘤(藍色)富集程度更高,但意外的是標(biāo)記曲妥珠的熒光物質(zhì)并沒有富集在HER2腫瘤表面、而是被運到免疫細(xì)胞富集的腫瘤邊緣。這可能是效率上抗原-抗體復(fù)合物被腫瘤內(nèi)吞輸給整個復(fù)合物被免疫細(xì)胞吞飲的一個例子。
抗體是經(jīng)過無數(shù)年演化篩選出來訓(xùn)練有素的分子,行為舉止十分規(guī)范、靶向不同抗原的同一類抗體進入人體后生老病死路徑都大差不差。這個平臺穩(wěn)定性令A(yù)DC可以持續(xù)產(chǎn)生藥物,而其它偶聯(lián)藥物如PDC可能每個產(chǎn)品都我行我素、結(jié)果更加難以預(yù)測。ADC能在萬物皆可偶聯(lián)時代一枝獨秀,成功率高于其它偶聯(lián)模式如SMDC、PDC與抗體經(jīng)過演化歷練獲得的組織紀(jì)律性不無關(guān)系。
美中藥源原創(chuàng)文章,轉(zhuǎn)載注明出處并添加超鏈接,商業(yè)用途需經(jīng)書面授權(quán)。★更多深度解析訪問《美中藥源》~
★ 請關(guān)注《美中藥源》微信公眾號 ★

發(fā)表評論
要發(fā)表評論,您必須先登錄。

















 微信號:美中藥源
微信號:美中藥源