ADC到底是什么?(二十四)多彈頭ADC

隨著優(yōu)質(zhì)ADC靶點(diǎn)的枯竭,很多人開始在毒素上做文章。一個(gè)方向是多彈頭ADC,一般是雙彈頭。當(dāng)然每個(gè)技術(shù)出現(xiàn)都會(huì)有人把它推向想象的極限,比如最近有一篇文章將多達(dá)六種不同類型的藥物負(fù)載到一個(gè)抗體上,藥物-抗體比(DAR)最高可達(dá)30 [1]。今天聊一聊多彈頭設(shè)計(jì)的骨感現(xiàn)實(shí)。
- 六個(gè)臭皮匠=臥龍+鳳雛?
雖然常言說(shuō)三個(gè)臭皮匠頂上一個(gè)諸葛亮,但臭皮匠也是有臭脾氣的、六個(gè)臭皮匠不等于同時(shí)擁有臥龍鳳雛。腫瘤確實(shí)是個(gè)多基因疾病,幾乎沒有一種腫瘤只用一種藥就可以控制、即使暫時(shí)控制也難免復(fù)發(fā)。因此腫瘤治療有很多治療方案是多藥聯(lián)用,但即使臨床使用的化療藥物組合疊加或協(xié)同作用也并不常見。2017年哈佛的科學(xué)家發(fā)現(xiàn),F(xiàn)DA批準(zhǔn)的組合療法應(yīng)答率高于單藥主要是因?yàn)閷?duì)多個(gè)藥物分別有應(yīng)答的患者在組合療法打擊下一次都應(yīng)答了,這種情況組合給藥和次序給藥區(qū)別不大(見圖一)[2]、但組合療法增加毒性概率和患者經(jīng)濟(jì)負(fù)擔(dān)。
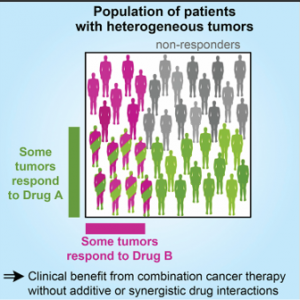
圖一
一個(gè)實(shí)操的障礙是已知單方的可能組合數(shù)量遠(yuǎn)遠(yuǎn)多于臨床上使用的組合療法,即組合爆炸難題。所以必須有臨床前高效篩選機(jī)制富集成功組合,否則不可能有足夠患者參加臨床試驗(yàn)來(lái)驗(yàn)證所有組合療法。多化療組合與單方比通常治療窗口并無(wú)改進(jìn),只是少數(shù)有改進(jìn)的組合保留下來(lái)了。諾華科學(xué)家根據(jù)小鼠PDX和預(yù)測(cè)模型估計(jì)只有<5%有單方活性的藥物組合可能會(huì)產(chǎn)生疊加或協(xié)同效應(yīng)[2,3],因?yàn)槿魏慰赡墚a(chǎn)生協(xié)同療效的組合都可能產(chǎn)生協(xié)同毒性,而且?guī)茁矢蟆o(wú)論對(duì)單方還是復(fù)方來(lái)說(shuō)毒性大于活性的化合物數(shù)量都遠(yuǎn)超有治療窗口的藥物(見圖二,黑色是預(yù)測(cè)會(huì)幫倒忙的組合、彩色是至少與單方同效組合[2])。
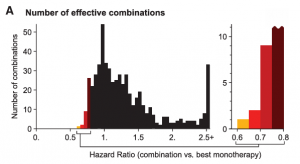
圖二
- 臨床前數(shù)據(jù)的轉(zhuǎn)化難題
雪上加霜的是pick the winner難題對(duì)單方和組合療法開發(fā)同樣適用,這少數(shù)可能獲益的組合有多少在臨床能轉(zhuǎn)化成患者收益還是未知數(shù)。盡管我們?cè)敢庀嘈潘幬锸窃O(shè)計(jì)出來(lái)的、至少是臨床前優(yōu)化體系篩選出來(lái)的,但一個(gè)扎心的事實(shí)是多數(shù)首創(chuàng)藥物是臨床篩選出來(lái)的,比紫杉醇抑制微管蛋白效果更好的化合物多如牛毛、但進(jìn)了臨床通通只有毒性、沒有活性。即使me-too藥物都不一定能在臨床前篩選,三個(gè)紫杉醇類藥物結(jié)構(gòu)變化很小、如同一人設(shè)計(jì),顯然設(shè)計(jì)者不相信篩選體系、不敢越雷池一步。有研究顯示組合療法臨床研究有一半沒有引用任何臨床前研究,基本就是盲篩。多彈頭ADC在人體的療效和安全性都無(wú)法在動(dòng)物實(shí)驗(yàn)可靠預(yù)測(cè)。
- ADC MTD由毒素決定
Colombo在2022年《Cancer Cell 》的那篇經(jīng)典綜述中比較令人信服地指出,在真正腫瘤患者ADC 的最大耐受劑量(MTD)往往與其所攜帶的小分子毒性藥物MTD相當(dāng)。我們以前分析過(guò)ADC雖然可能選擇性在腫瘤釋放毒素、但這只占總藥量的1%不到,>99%毒素在正常組織釋放、這些毒素最終要回到血液才能被人體清除。所以攜帶毒素的總量ADC比小分子藥物并無(wú)太大區(qū)別,比如Trodelvy比伊利替康的血液SN38 AUC還高十幾倍、較起真來(lái)誰(shuí)是更魔法的子彈還不好說(shuō)。如果單彈頭ADC的MTD與毒素類似,沒有理由懷疑多彈頭ADC有什么不同。
- PK同步嗎?
多彈頭ADC因?yàn)槎舅囟荚谝粋€(gè)分子上理論上實(shí)現(xiàn)了毒素釋放的“PK同步”,但幾乎所有ADC 毒素在腫瘤之外組織釋放并最終回到血液、與小分子組合靜脈滴注對(duì)于外周毒性(ADC的主要毒性)不會(huì)有顯著差別。ADC依賴非平衡藥物分布、與小分子系統(tǒng)給藥通過(guò)血液與各組織達(dá)到分布平衡的工作機(jī)制不同,不同毒素組織逃逸動(dòng)、旁觀者效應(yīng)(過(guò)膜性)、腫瘤殺傷動(dòng)力學(xué)的差異會(huì)嚴(yán)重影響腫瘤殺傷疊加作用。另外因?yàn)橹挥猩倭慷舅卦谀[瘤和在靶脫組織釋放,所以各個(gè)毒素在腫瘤比例的個(gè)體差異比血液循環(huán)的個(gè)體差異要大。這可能導(dǎo)致外周毒性穩(wěn)定地與化療組合類似,但腫瘤療效和在靶毒性卻個(gè)體或整體差異都很大。
- 高DAR 的開發(fā)挑戰(zhàn)
高于DAR 8的ADC已被認(rèn)為開發(fā)難度巨大,DAR20-30就更難了。負(fù)載越多,分子越疏水,越容易聚集,即便使用疏水性掩蓋等技術(shù)也難以完全解決這一問題。高DAR引起的免疫原性也是問題,CMC復(fù)雜度也會(huì)幾何級(jí)增長(zhǎng)、每添加一種新毒素就意味著新增一系列雜質(zhì)譜和質(zhì)控點(diǎn)。
- 多靶點(diǎn)藥物的教訓(xùn)
很多癌癥治療方案依賴聯(lián)合用藥,但將“聯(lián)合用藥”轉(zhuǎn)化為“共軛用藥”卻成功率不高。組合療法依賴靈活性,即藥物劑量可調(diào)、可停、可錯(cuò)峰投用,而當(dāng)六種藥物被永久性地綁在一個(gè)抗體上后,劑量調(diào)節(jié)的空間就不存在了。多彈頭ADC并不是第一次嘗試多靶點(diǎn)共價(jià)化設(shè)計(jì),多靶點(diǎn)小分子藥(multiple ligands)幾十年前就是一個(gè)熱門領(lǐng)域,但盡管臨床前看著不錯(cuò)但臨床只有少數(shù)如bendamustine的成功案例。一旦一個(gè)成分的毒性限制了劑量,其他藥物也隨之被“綁架”,只能在亞治療劑量下發(fā)揮作用。確實(shí)有些機(jī)理可以被很低劑量第二個(gè)組分曾敏,但這和開發(fā)FIC沒有什么本質(zhì)區(qū)別。
- Pipeline in a drug
有些藥物如修美樂、K藥適應(yīng)癥多,每個(gè)適應(yīng)癥開發(fā)成功幾率高,所以被叫做pipeline in a drug,但把多個(gè)藥物共價(jià)鏈接成一個(gè)藥物難以復(fù)制這個(gè)理念。根據(jù)化療的經(jīng)驗(yàn),次序使用不同毒素的ADC可能是更可控、更安全的策略。
小結(jié)
組合療法開發(fā)的障礙也同樣是多毒素ADC開發(fā)的障礙,可能的組合太多、但有疊加協(xié)同效應(yīng)組合很少,臨床前沒有可靠的篩選系統(tǒng)。化療的治療窗口都很小,不是1也達(dá)不到2、沒有多少出錯(cuò)空間,所以如果固定比例不能調(diào)節(jié)劑量和給藥頻率自縛手腳就更難找到獲勝組合。次序使用ADC已經(jīng)是臨床實(shí)踐,至少短期內(nèi)這可能是更可靠、更安全的利用不同毒素的策略。
參考文獻(xiàn):
[1] Meng, Xun, et al. "Antibody-mediated co-delivery of programmable drug combinations." (2024).
[2] Palmer, Adam C., and Peter K. Sorger. "Combination cancer therapy can confer benefit via patient-to-patient variability without drug additivity or synergy." Cell 171.7 (2017): 1678-1691.
[3] Gao, Hui, et al. "High-throughput screening using patient-derived tumor xenografts to predict clinical trial drug response."?Nature medicine?21.11 (2015): 1318-1325.
美中藥源原創(chuàng)文章,轉(zhuǎn)載注明出處并添加超鏈接,商業(yè)用途需經(jīng)書面授權(quán)。★更多深度解析訪問《美中藥源》~
★ 請(qǐng)關(guān)注《美中藥源》微信公眾號(hào) ★

發(fā)表評(píng)論
要發(fā)表評(píng)論,您必須先登錄。


















 微信號(hào):美中藥源
微信號(hào):美中藥源