

Alnylam的Givosiran(商品名Givlaari)今天被FDA批準(zhǔn)用于一種叫做急性肝卟啉病(AHP)的超級罕見病,成為第二個在美國上市的RNAi藥物。這個批準(zhǔn)是根據(jù)一個叫做ENVISION的三期臨床試驗,
Continue reading …
今天Bloomberg News報道諾華可能收購開發(fā)PCSK9 RNAi藥物inclisiran的Medicines Company,令今天MDCO股票上揚20%。
Continue reading …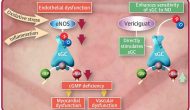
今天默沙東與合作伙伴拜耳宣布其心衰藥物、可溶性鳥苷酸環(huán)化酶(sGC)激動劑Vericiguat在一個叫做VICTORIA的國際多中心三期臨床試驗達到由心衰住院和心血管死亡組成的復(fù)合一級終點。
Continue reading …
昨天FDA專家組以16:0全票支持將Amarin的純EPA魚油制劑Vascepa標(biāo)簽擴展到心血管預(yù)防,礦物油作為安慰劑并未令專家組質(zhì)疑關(guān)鍵試驗Reduce-it結(jié)果的可靠性,但專家對是否將標(biāo)簽限制在二級預(yù)防、出血和心率不齊危險等進行了討論。
Continue reading …
今天FDA通過加速審批通道批準(zhǔn)了百濟神州的BTK抑制劑Brukinsa (通用名zanubrutinib)用于治療至少失敗一種療法的套細胞淋巴瘤。這個審批是根據(jù)一個86人參與的單臂臨床試驗結(jié)果,Brukinsa在這個人群的應(yīng)答率為84%、中值應(yīng)答時間為19.5個月。
Continue reading …
今天羅氏宣布SMA患者使用一年其小分子藥物risdiplam比安慰劑顯著改善2-25歲2、3型SMA患者的運動功能、并且沒有發(fā)現(xiàn)嚴重藥物相關(guān)副作用
Continue reading …
今天在SITC年會上匹斯堡大學(xué)的Kirkwood教授匯報了Checkmate Pharmaceutical的TLR9激動劑CMP-001單方或與K藥組合在K藥耐藥惡黑患者的一個二期臨床結(jié)果。
Continue reading …
今天美國衛(wèi)生部向法庭提出訴訟指控吉利德科學(xué)使用其艾滋病藥物Truvada和Descovy用于感染前預(yù)防(PrEP)侵犯了CDC在2015年獲得的一項用途專利
Continue reading …
今天百健宣布擴大與韓國生物技術(shù)藥企業(yè)三星生物的合作,以1億美元首付、2.1億美元里程金獲得視網(wǎng)膜疾病藥物雷珠單抗(商品名Lucentis)和阿柏西普(商品名Eylea) 生物類似藥(分別叫做SB11、SB15)在歐美、日本等幾個主要 市場的權(quán)益。同時百健還將獲得二者合作的三個TNF藥物在中國市場的權(quán)益。兩個公司的聯(lián)合公司Samsung Bioepis將負責(zé)這兩個藥物的臨床開發(fā)。
Continue reading …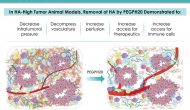
今天美國生物技術(shù)公司Halozyme宣布其透明質(zhì)酸酶制劑PEGPH20在一個叫做HALO-301的胰腺癌三期臨床失敗。這個試驗在吉西他濱和ABRAXANE?背景上比較PEGPH20與安慰劑作為晚期胰腺癌一線藥物對OS的影響,
Continue reading …
今天諾華SMN1基因療法Zolgensma的兩個臨床試驗被FDA部分叫停。一個叫做STRONG的臨床試驗低劑量組已經(jīng)結(jié)束、將停止招募和使用高劑量Zolgensma。
Continue reading …
今天美國生物技術(shù)公司Mirati在 EORTC-NCI-AACR年會上公布了其G12C變異Kras藥物MRTX849的首批臨床數(shù)據(jù)。在6位使用最高劑量MRTX849(600毫克一日兩次)的NSCLC患者中有3位達到部分應(yīng)答、但有2例尚未經(jīng)中心機構(gòu)確認。四位高劑量CRC患者有一例應(yīng)答、并已經(jīng)確認。首次消息影響MRTX股票上揚22%。
Continue reading …
APOE基因E4變異是最主要的老年癡呆癥風(fēng)險變異,攜帶一條E4變異的人群,罹患老年癡呆癥的風(fēng)險增加3-4倍,而攜帶二條E4變異,得病風(fēng)險增加12-15倍。
Continue reading …
今天《自然》雜志發(fā)表了芝加哥大學(xué)趙英明教授小組的一篇表觀遺傳蛋白修飾文章,首次揭示了組蛋白賴氨酸乳酸酰化(Kla)這個調(diào)控機制,并證明其在基因表達,微環(huán)境中改變巨噬細胞中的作用。作者首先用一系列化學(xué)和生化的方法,
Continue reading …
今天百健與合作伙伴衛(wèi)材宣布其粉狀蛋白抗體aducanumab的高劑量組(10毫克)在一個叫做Emerge的阿爾茨海默病三期臨床試驗中顯著改善一個叫做CDR-SB的評分指標(biāo),
Continue reading …
今天FDA批準(zhǔn)了福泰的囊腫性肺纖維化(CF)三藥組合Trikafta(elexacaftor, tezacaftor,ivacaftor)用于12歲以上、CFTR至少有一種F508del型變異的CF患者。這個審批是根據(jù)兩個三期臨床的陽性結(jié)果,
Continue reading …




















 微信號:美中藥源
微信號:美中藥源