
美國FDA同意 Aeterna Zentaris制藥公司的AEZS-108三期臨床使用“特殊評估方案”
作者:朱貴東
據(jù)PR Newswire 12月28日報道,Aeterna Zentaris制藥公司公布美國食品藥品監(jiān)督管理局(FDA)同意其候選藥AEZS-108的三期臨床使用“特殊評估方案”(special protocol assessment, SPA)。按照該SPA協(xié)議,F(xiàn)DA允許Aeterna Zentaris的新藥申報(NDA)采用一個隨機(jī)、多中心三期臨床的設(shè)計方案、實驗終點和數(shù)據(jù)統(tǒng)計,頭對頭比較AEZS-108和阿霉素作為二線藥物治療局部晚期,復(fù)發(fā)或轉(zhuǎn)移性子宮內(nèi)膜癌。
“特殊評估方案”是美國FDA接受不完整的三期臨床實驗設(shè)計、實驗終點和數(shù)據(jù)統(tǒng)計作為新藥申報(NDA)組成部分的聲明。最終審批依然取決于候選藥的療效、不良反應(yīng)以及獲益/風(fēng)險評估。
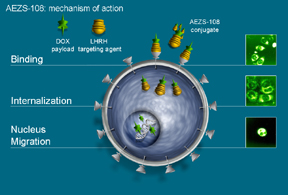
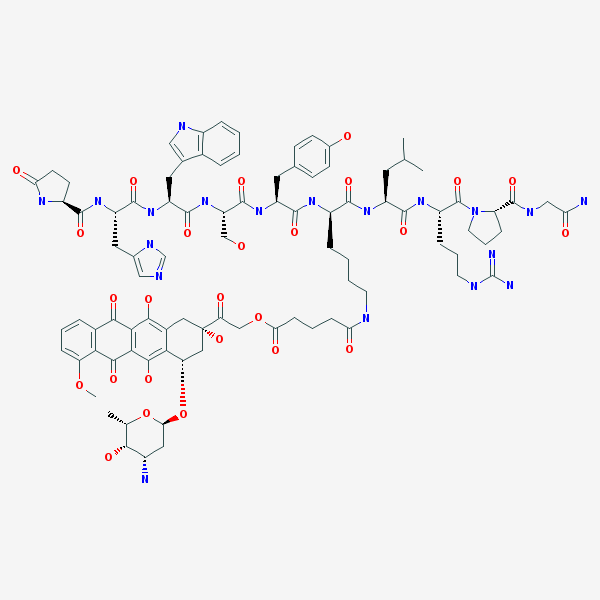
AEZS-108是一種新型靶向型抗腫瘤藥物,把阿霉素和一個靶向促黃體激素釋放激素(LHRH)受體的多肽連接(見下圖化學(xué)結(jié)構(gòu)),主要用于治療對LHRH高表達(dá)的卵巢癌、子宮內(nèi)膜癌、前列腺癌、乳腺癌和膀胱癌等。因為多肽和腫瘤細(xì)胞表面LHRH受體的親和作用,導(dǎo)致AEZS-108在腫瘤細(xì)胞內(nèi)的融合和富集作用,從而有效地提高了偶聯(lián)物的靶向性。美國和歐共體藥物監(jiān)管部分已經(jīng)授予AEZS-108的孤兒藥地位。
11月18日,Aeterna Zentaris在柏林舉行的第22屆EORTC-NCI-AACR分子標(biāo)靶和癌癥治療研討會上公布AEZS-108的一個注冊有43位晚期或復(fù)發(fā)子宮內(nèi)膜癌患者的二期臨床實驗結(jié)果。患者每三周注射每平方米267毫克的AEZS-108,共六次。一級實驗終點是患者的應(yīng)答率,二級終點是不良反應(yīng)、疾病進(jìn)展的中位數(shù)和最終生存率。結(jié)果發(fā)現(xiàn),有2位患者取得完全應(yīng)答,占5.1%;10位病人達(dá)到部分應(yīng)答,占25.6%;17為患者病情沒有惡化,占43.6%。最終存活率和進(jìn)展中位數(shù)分別為14.3和7個月,優(yōu)于鉑類抗癌藥和紫杉醇類抗癌藥的歷史療效。
美中藥源原創(chuàng)文章,轉(zhuǎn)載注明出處并添加超鏈接,商業(yè)用途需經(jīng)書面授權(quán)。★更多深度解析訪問《美中藥源》~
★ 請關(guān)注《美中藥源》微信公眾號 ★

發(fā)表評論
要發(fā)表評論,您必須先登錄。

















 微信號:美中藥源
微信號:美中藥源