美國FDA批準(zhǔn)拜耳Adempas(riociguat)用于治療肺動(dòng)脈高壓
作者:佚名
10月8日,美國食品藥品管理局(FDA)批準(zhǔn)Adempas(通用名:Riociguat)用于治療成人兩種形式的肺動(dòng)脈高壓。肺動(dòng)脈高壓由肺部動(dòng)脈異常高血壓引起。該病癥使右側(cè)心臟工作起來比正常情況更艱難。在其各種疾病形式中,肺動(dòng)脈高壓是一種慢性、進(jìn)展性并使人衰弱的疾病,常常會(huì)導(dǎo)致死亡或需要肺移植。
Adempas屬于一類叫做可溶性鳥苷酸環(huán)化酶激活劑的藥物,這類藥物有助于動(dòng)脈松弛,從而使血流增加,血壓降低。這款藥物旨在治療術(shù)后慢性血栓栓塞性肺動(dòng)脈高壓(CTEPH)患者或無法接受手術(shù)的患者,以改善他們的運(yùn)動(dòng)能力。Adempas也用于治療不明原因引起的、遺傳性的或與結(jié)締組織病有關(guān)的肺動(dòng)脈高壓(PAH)患者,以改善患者的運(yùn)動(dòng)能力并推遲他們疾病的臨床惡化進(jìn)度。
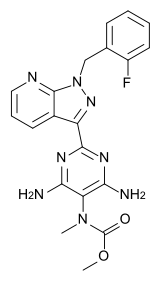
Riociguat的化學(xué)結(jié)構(gòu):
“Adempas是可溶性鳥苷酸環(huán)化酶激活劑中首款獲批用于治療肺動(dòng)脈高壓的藥物,也是首款證明對(duì)CTEPH患者有效的藥物。”FDA藥物評(píng)價(jià)與研究中心心血管與腎病藥物產(chǎn)品部門主任、醫(yī)學(xué)博士與理學(xué)博士Norman Stockbridge說。FDA是在優(yōu)先審評(píng)計(jì)劃下完成Adempas審評(píng)的,優(yōu)先審評(píng)可以為治療上能提供重要進(jìn)展的藥物提供一個(gè)加快的6個(gè)月的審評(píng)。
Adempas治療CTEPH的安全性和有效性基于一項(xiàng)由261名受試者參與的臨床試驗(yàn),試驗(yàn)中受試者被隨機(jī)配給Adempas,用藥劑量逐漸增加到2.5mg,每天用藥三次,或配給安慰劑每天使用三次。這項(xiàng)研究的目的是檢測受試者6分鐘之內(nèi)所能行走距離的變化。經(jīng)過16周的治療后,Adempas用藥患者6分鐘行走距離平均增加46米,遠(yuǎn)超過安慰劑治療患者。
用來評(píng)價(jià)Adempas治療PAH安全性和有效性的臨床試驗(yàn)由443名受試者參與,患者被隨機(jī)配給1.5mg或2.5mg劑量的Adempas或者安慰劑,每天用藥三次。經(jīng)過16周治療后,Adempas用藥患者6分鐘行走距離平均提高36米,遠(yuǎn)超過安慰劑治療患者。
Adempas藥品標(biāo)簽中帶有一項(xiàng)黑框警告,提示患者與衛(wèi)生保健專業(yè)人員這款藥物不能用于孕婦,因?yàn)樗鼤?huì)傷害胎兒的發(fā)育。女性患者只能通過Adempas風(fēng)險(xiǎn)評(píng)估與降低(REMS)計(jì)劃來獲取這款藥物。所有女性患者必須加入這個(gè)計(jì)劃,遵守懷孕測試要求,并得到需要進(jìn)行避孕的勸告。限制藥品分銷的REMS計(jì)劃要求開處方者加入該項(xiàng)計(jì)劃并獲得認(rèn)證。同時(shí),藥店必須通過認(rèn)證并只能將這款藥物分發(fā)給按REMS要求有資格使用的患者。
Adempas治療患者常見的副作用包括頭痛、頭暈、消化不良、組織腫脹(外圍性水腫)、惡心、腹瀉和嘔吐。Adempas由位于新澤西州韋恩的拜耳醫(yī)藥保健制藥公司上市銷售。
美中藥源原創(chuàng)文章,轉(zhuǎn)載注明出處并添加超鏈接,商業(yè)用途需經(jīng)書面授權(quán)。★更多深度解析訪問《美中藥源》~
★ 請(qǐng)關(guān)注《美中藥源》微信公眾號(hào) ★

發(fā)表評(píng)論
要發(fā)表評(píng)論,您必須先登錄。


















 微信號(hào):美中藥源
微信號(hào):美中藥源