_藥源搜索

美國FDA批準(zhǔn)Valeant制藥公司的Luzu? (luliconazole Cream) 用于治療真菌感染引起的常見皮膚病
作者:佚名
Valeant制藥公司于 11月15日宣布,其全資附屬的Valeant制藥北美公司已收到美國FDA通知,批準(zhǔn)Luzu? ( luliconazole Cream,盧立康唑霜1%)的新藥申請,用于治療18歲及以上足癬,紅色毛癬菌和絮狀表皮癬菌等癬菌引起的股癬患者。這些都是主要由皮膚真菌引起常見皮膚疾病。
該公司的董事長兼首席執(zhí)行官J. Michael Pearson說:“我們很高興LUZU?比預(yù)期的提前獲得FDA的批準(zhǔn)。 這是第一個安全和有效的治療周期為一周的日用藥品,比起現(xiàn)在為期兩周的治療方案,這將是一個會受歡迎的替代治療選擇,我們相信LUZU?將使我們很好地解決這一日益嚴(yán)重的未滿足的治療需求。”
LUZU?(盧立康唑)霜(1%),是為期一周,每日一次的治療方案,適應(yīng)癥為股癬和皮膚癬,是目前唯一的治療周期為一周的外用唑類抗真菌劑。所有其他經(jīng)批準(zhǔn)的治療方案都需要進(jìn)行為期兩個星期的治療。針對指狀組合型腳癬需要每日一次為期兩周的治療。美國是北美首個批準(zhǔn)的國家。盧立康唑已經(jīng)于2005年已在在日本被批準(zhǔn)上市。
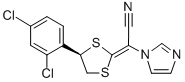
Luliconazole的化學(xué)結(jié)構(gòu)為:
美中藥源原創(chuàng)文章,轉(zhuǎn)載注明出處并添加超鏈接,商業(yè)用途需經(jīng)書面授權(quán)。★更多深度解析訪問《美中藥源》~
★ 請關(guān)注《美中藥源》微信公眾號 ★

發(fā)表評論
要發(fā)表評論,您必須先登錄。


















 微信號:美中藥源
微信號:美中藥源