MTH1有望成為新一代有效抗癌分子靶點
作者:呂順
【新聞背景】來自瑞典、奧地利和德國的三個不同聯(lián)合研究小組最近分別在《自然》和《應用化學》雜志上發(fā)表論文,證明細胞內(nèi)負責清理氧化性損傷堿基的一種酶—MTH1(又稱NUDT1)可能是一個新一代有效抗癌分子靶點。MTH1通常被認為起著“消毒劑”的作用,能有效地阻止受氧化損傷的脫氧核糖核酸苷摻入到DNA。這三個研究組各自獨立地通過不同研究手段,比如采用shRNA或小分子抑制劑下調(diào)這種酶的活性,發(fā)現(xiàn)抑制MTH1能導致癌細胞發(fā)生致死性的DNA雙鏈斷裂和細胞凋亡,而且這個現(xiàn)象被多個動物實驗所證實,指出MTH1有望成為新一代的有效抗癌分子靶點。
【藥源解析】眾所周知,新藥研發(fā)的過程復雜而漫長,不僅耗資數(shù)十億美元且涉及很多學科以及學術(shù)以外的因素。本站多次闡述,如果剝離所有技術(shù)細節(jié),靶點的發(fā)現(xiàn)和確證是現(xiàn)代新藥研發(fā)的瓶頸和核心。也就是說,一旦知道哪個靶點確實有效,目前的藥物化學、藥理、毒理、臨床開發(fā)技術(shù)水平可以快速地發(fā)現(xiàn),開發(fā)針對這個分子靶點的新藥。在抗腫瘤研究領域,近幾十年來通過靶向腫瘤的特異特征,尤其是靶向癌細胞中的特異遺傳缺陷,發(fā)現(xiàn)了以BCR-ABL、ALK為代表的一系列優(yōu)質(zhì)分子靶點,開發(fā)了伊馬替尼、克里唑替尼等靶向抗癌藥物。但是更多的分子靶點后來未能在臨床上被證實,一些上市的抗癌藥還出現(xiàn)耐藥性,在使用一段時間以后不再顯示療效。
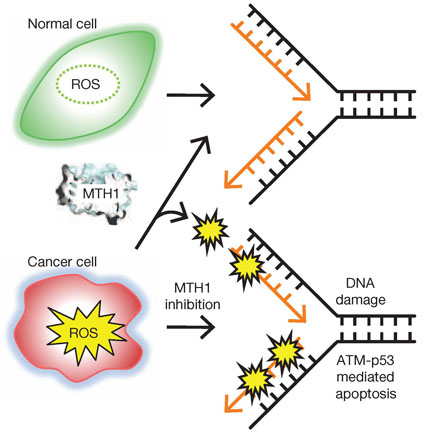
如上圖所示,細胞代謝會產(chǎn)生活性氧(Reactive Oxygen Species,ROS),活性氧能快速地氧化脫氧核苷三磷酸(dNTP),其反應速率比對雙螺旋DNA中的堿基要高出數(shù)千倍。如果氧化的dNTP摻入到DNA中,不僅會造成基因組不穩(wěn)定,產(chǎn)生突變,更會發(fā)生致死性的DNA雙鏈斷裂與細胞凋亡。生物機體相應地進化,產(chǎn)生了針對這一問題的解決辦法——MTH1酶。因為癌細胞的增殖遠遠快于正常細胞,產(chǎn)生更多的活性氧并需要大量的脫氧核苷單體。MTH1通過水解dNTP的氧化形式,比如8-oxo-dGTP 和2-OH-dATP,將它們轉(zhuǎn)化成不能用于DNA合成的磷酸產(chǎn)物,也就是說MTH1酶能通過選擇性清除NTP池中的氧化核苷酸,充當損傷堿基的“消毒劑”,阻止了DNA構(gòu)件的氧化形式摻入到DNA中,確保了癌細胞的復制過程,使得它們能夠進行持續(xù)分裂和大量增殖。
以Karolinska學院Thomas Helleday為首的,包括瑞典5所大學的聯(lián)合研究團隊在《自然》發(fā)表文章指出,所有測試的癌細胞都因ROS水平過高而依賴MTH1酶來維持生存。而正常細胞不同,無需MTH1酶的存在。尤其有意思的是,MTH1酶的活性和特定癌癥中的遺傳變異沒有相關性。這樣,MTH1在癌細胞中扮演了關鍵的氧化還原適應作用,而MTH1抑制劑能靶向這個癌細胞特異的氧化還原適應機制,為癌癥治療提出一種新策略。更可貴的是該氧化還原適應機制獨立于癌細胞的遺傳變異,從而不會導致因治療產(chǎn)生的耐藥性。Helleday課題組還制作了一個動畫,闡述了MTH1抑制劑通過下調(diào)MTH1酶的活性,促使受損核苷酸摻入DNA的合成,由此造成DNA損傷并殺死癌細胞的過程。而正常細胞不需要MTH1,可以通過調(diào)控新陳代謝來阻止核苷酸構(gòu)件的損害。這樣發(fā)現(xiàn)了癌細胞和正常細胞在氧化還原適應機制中的區(qū)別,為治療癌癥開辟了一條全新的途徑。
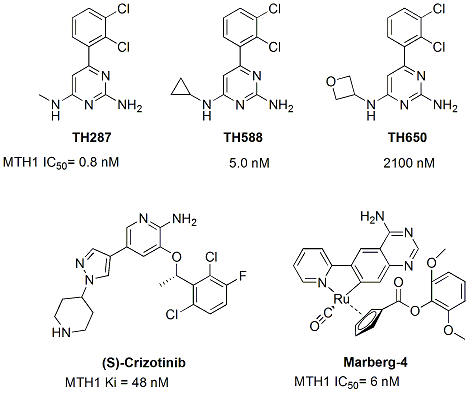
如上圖所示,Helleday課題組通過晶體結(jié)構(gòu)分析、高通量篩選和構(gòu)效關系研究,不僅找到了MTH1蛋白的兩個結(jié)合位點,還發(fā)現(xiàn)了包括TH287、TH588在內(nèi)的MTH1抑制劑。其中后者還展現(xiàn)較好的藥物動力學特征。體外實驗說明,這些MTH1抑制劑對多種癌細胞能導致和劑量/活性相關的dNTP氧化、DNA損傷以及細胞毒性,但在正常細胞中卻沒有反應。小鼠接種實驗(xenograft)證明,TH588不僅對結(jié)腸癌(SW480)和乳腺癌(MCF7),而且對多種藥物耐藥的皮膚癌顯示療效。奧地利科學院分子醫(yī)學研究中心的Giulio Superti-Furga研究小組則另辟蹊徑,發(fā)現(xiàn)2011年批準的一類肺癌藥物crizotinib(克里唑替尼)的手性對映體(S-crizotinib)也抑制MTH1酶的活性,并在動物實驗中顯示療效。MTH1酶作為一個潛在抗癌靶點在抗癌戰(zhàn)爭中的作用還被德國Marberg大學的Margherita Bignami研究團隊通過合成包括Marberg-4化合物在內(nèi)的一組金屬MTH1抑制劑證實。
毫無疑問,MTH1作為一個有效抗癌靶點還要做大量的工作,甚至按照大型制藥企業(yè)的標準距離臨床上認證也還差很遠。《美中藥源》之前曾詳細討論過,靶點認證的“假陽性”或“假陰性”經(jīng)常誤導新藥開發(fā),很多人認為至少有一半以上發(fā)表的生物學研究結(jié)果不能按照工業(yè)界的標準被重復,比如斯坦福大學的Loannidis教授在2005年曾報道,在45個被高度頻繁引用的臨床研究中只有20個能被重復,有14個結(jié)論后來證明是是錯的或夸大的,11個無后續(xù)研究驗證起真實性。但是,來自瑞典、奧地利和德國三個不同課題組,各自獨立地證明MTH1抑制劑能有效地殺死癌細胞并在動物模型中顯示療效。這樣,這三個研究又從不同側(cè)面互相驗證了對方的實驗結(jié)果,顯著降低了因為偶然因素導致實驗結(jié)果的“假陽性”,說明如果動物實驗能轉(zhuǎn)化到人體,MTH1應該是一個有效靶點。
當然在臨床開發(fā)之前,這些MTH1抑制劑還要進一步被結(jié)構(gòu)優(yōu)化,改良它們的藥效、毒理以及成藥特征。根據(jù)報道的構(gòu)效關系,比如在TH287、TH588、TH650等化合物中隨著氨基上烷基體積的增加,MTH1的抑制活性明顯降低,克里唑替尼(crizotinib)和其S-對映體相比抑制MTH1酶的活性要低20倍以上,暗示這些抑制劑不僅對MTH1顯示明顯的構(gòu)效關系,也極具被優(yōu)化成理想抗癌候選藥的潛力。但是筆者也認為,癌細胞增殖對氧化還原適應機制是否完全依賴還有待進一步驗證,在很大程度上MTH1可能更是其它靶向藥物的增敏劑,且在以上獨立的動物實驗中都未能清除腫瘤也略見一斑,聯(lián)合用藥或許是開發(fā)MTH1抑制劑更大的機會。
美中藥源原創(chuàng)文章,轉(zhuǎn)載注明出處并添加超鏈接,商業(yè)用途需經(jīng)書面授權(quán)。★更多深度解析訪問《美中藥源》~
★ 請關注《美中藥源》微信公眾號 ★

發(fā)表評論
要發(fā)表評論,您必須先登錄。


















 微信號:美中藥源
微信號:美中藥源