美國(guó)FDA一個(gè)月內(nèi)批準(zhǔn)的第二個(gè)抗菌素新藥Sivextro預(yù)示抗生素新藥研發(fā)的春天?
作者:呂順
【新聞事件】6月20日下午,一種新的惡唑烷酮類抗菌素Sivextro(tedizolid phosphate,磷酸泰地唑胺)獲得美國(guó)FDA批準(zhǔn),用于治療金黃色葡萄球菌(包括耐甲氧西林菌株、甲氧西林敏感菌株)和各種鏈球菌屬和糞腸球菌等革蘭氏陽(yáng)性細(xì)菌引起的急性細(xì)菌性皮膚和皮膚結(jié)構(gòu)感染(ABSSSI)。這是FDA繼5月23日批準(zhǔn)Dalvance(dalbavancin,達(dá)巴萬(wàn)星)之后批準(zhǔn)用于治療ABSSSI感染的第二個(gè)抗菌素新藥。
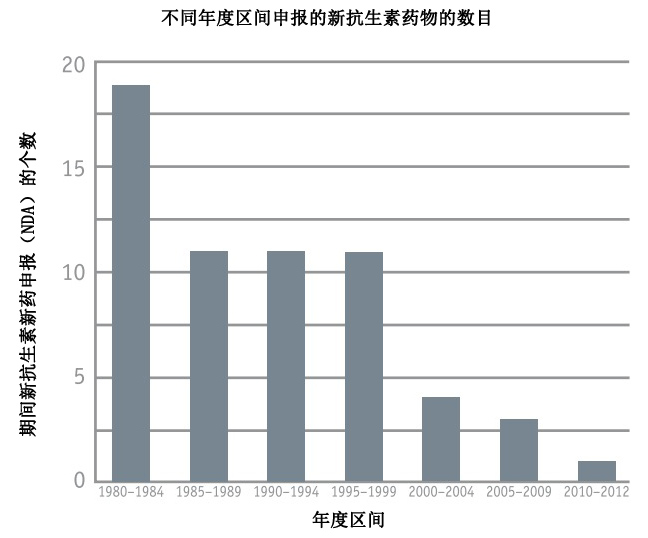
【藥源解析】抗菌素是臨床上使用最頻繁的基本藥物之一。由于歷史原因造成的抗生素不規(guī)范使用,造成細(xì)菌對(duì)現(xiàn)有抗生素嚴(yán)重的抗藥性。多藥耐藥(MDR)的細(xì)菌感染已經(jīng)成為全球公共健康的主要威脅之一。正因?yàn)槎嗨幠退帲咕氐穆?lián)合用藥也日趨增多,藥物-藥物相互作用也增加了不良反應(yīng)的發(fā)生風(fēng)險(xiǎn)。根據(jù)最近國(guó)家食藥監(jiān)總局發(fā)布的2013年國(guó)家藥品不良反應(yīng)監(jiān)測(cè)年度報(bào)告,由抗菌素引起的不良反應(yīng)高居不良反應(yīng)/事件報(bào)告的首位。對(duì)目前絕大多數(shù)可用的抗生素都有抗藥性的“超級(jí)細(xì)菌”也以驚人的速度在世界范圍蔓延,。另一方面,新型有效的抗生素研發(fā)并沒(méi)有伴隨MDR細(xì)菌的增加而增加。根據(jù)美國(guó)FDA新藥評(píng)價(jià)中心(CDER)的數(shù)據(jù),自1980年以來(lái)新批準(zhǔn)的抗生素?cái)?shù)量反而在不斷減少(見(jiàn)下圖)。現(xiàn)有的抗菌素已經(jīng)無(wú)法治愈日益增加的感染和耐藥。
為了開(kāi)發(fā)新型、有效的抗生素,控制多藥耐藥細(xì)菌的擴(kuò)散以及保護(hù)公共健康的安全,現(xiàn)行抗生素激勵(lì)(GAIN)條款作為美國(guó)FDA安全與創(chuàng)新法案的一部分也被寫(xiě)入法律,那些獲得合格傳染病產(chǎn)品(Qualified Infectious Disease Product,QIDP)認(rèn)證的,用于治療嚴(yán)重或危及生命感染的藥物在獲得食品,藥品和化妝品法規(guī)定的(市場(chǎng))排他期之外還享有額外5年的市場(chǎng)獨(dú)占權(quán)。自此,抗生素藥物的開(kāi)發(fā)有明顯增加的趨勢(shì)。美國(guó)傳染病協(xié)會(huì)(IDSA)已經(jīng)和數(shù)十家機(jī)構(gòu)合作,致力于10x20方案,目標(biāo)在2020年能開(kāi)發(fā)10個(gè)新的抗生素藥物。
Sivextro(通用名:tedizolid磷酸鹽,曾用名:TR-701)由Cubist制藥公司開(kāi)發(fā),是一種惡唑烷酮類抗生素。Sivextro是一種前藥,在體內(nèi)可被磷酸酶迅速轉(zhuǎn)化為具有生物活性的tedizolid。后者能夠和細(xì)菌的核糖體50S亞基結(jié)合,從而抑制蛋白質(zhì)的合成。盡管自2000年輝瑞的同類抗菌素利奈唑胺獲得美國(guó)FDA批準(zhǔn)以后,至少有10個(gè)同類化合物進(jìn)入臨床,但Sivextro是第一個(gè)獲得FDA批準(zhǔn)的二代惡唑烷酮類抗生素。和一代產(chǎn)品利奈唑胺相比,Sivextro對(duì)一些細(xì)菌的體外抑制活性要高2-8倍,安全性在一定程度上也有所提高。
在一個(gè)最近發(fā)表在《柳葉刀》上的雙盲三期臨床實(shí)驗(yàn)中(ESTABLISH-2實(shí)驗(yàn)),667例懷疑或確認(rèn)患有革蘭氏陽(yáng)性細(xì)菌感染的成人患者被隨機(jī)分為Sivextro治療組和現(xiàn)行金標(biāo)利奈唑胺陽(yáng)性對(duì)照組。Sivextro治療組連續(xù)6天,每天一次口服200毫克的Sivextro和對(duì)照組連續(xù)10天,每天兩次口服600毫克的利奈唑胺相比療效無(wú)明細(xì)區(qū)分。在口服治療之前,所有患者都接受短期的Sivextro或利奈唑胺的靜脈輸液治療。在另一個(gè)有566位患者參與的三期實(shí)驗(yàn)中(NCT02066402),采用Sivextro和利奈唑胺治療48-72小時(shí)后,治療組和對(duì)照組的病灶面積都下降20%以上,達(dá)到一級(jí)實(shí)驗(yàn)終點(diǎn)。
2013年12月13日,Sivextro獲得FDA的優(yōu)先審查資格,處方藥用戶收費(fèi)法(PDUFA)目標(biāo)日期為2014年6月20日。2014年4月14日,F(xiàn)DA抗感染藥物顧問(wèn)委員會(huì)(AIDAC)以14:0的一致投票建議批準(zhǔn)Sivextro。
美中藥源原創(chuàng)文章,轉(zhuǎn)載注明出處并添加超鏈接,商業(yè)用途需經(jīng)書(shū)面授權(quán)。★更多深度解析訪問(wèn)《美中藥源》~
★ 請(qǐng)關(guān)注《美中藥源》微信公眾號(hào) ★

發(fā)表評(píng)論
要發(fā)表評(píng)論,您必須先登錄。


















 微信號(hào):美中藥源
微信號(hào):美中藥源