默克首創(chuàng)PD-1抑制劑Keytruda(pembrolizumab)能領(lǐng)銜黑色素瘤市場(chǎng)嗎?
作者:呂順
藥源剛剛討論過,PD-1抑制劑的橫空出世對(duì)黑色素瘤乃至整個(gè)抗腫瘤藥物的開發(fā)有著深遠(yuǎn)的影響。默克和施貴寶的投資力度、開發(fā)策略、臨床設(shè)計(jì)、以及上市申報(bào)都堪稱完美,成為現(xiàn)代新藥開發(fā)的金標(biāo)。施貴寶的PD-1抑制劑nivolumab(商品名:Opdivo)率先在日本上市,用于治療晚期黑色素瘤。默克的pembrolizumab(商品名:Keytruda)是在美國(guó)第一個(gè)上市的PD-1抑制劑,治療已經(jīng)接受過ipilimumab治療但仍有進(jìn)展,或?qū)pilimumab和BRAF抑制劑雙重耐藥的BRAF V600基因變異的晚期黑色素瘤患者。Keytruda從招募第一個(gè)受試者到獲得PDA的加速批準(zhǔn)僅僅花費(fèi)了3年左右的時(shí)間,按照福布斯Matthew Herper的話說(shuō)“如果再有人向你說(shuō)因監(jiān)管復(fù)雜導(dǎo)致抗癌藥的審批總是緩慢、艱難的話,默克的pembrolizumab就是一個(gè)反證”。
我們也多次討論過,現(xiàn)代制藥工業(yè)me-too類藥物的開發(fā)在多數(shù)疾病領(lǐng)域漸漸失去競(jìng)爭(zhēng)力,大多數(shù)制藥巨頭主要的研發(fā)投入逐漸向具有突破性的新療法傾斜。比如默克花重金確保pembrolizumab走在PD-1開發(fā)的前列,其研發(fā)總監(jiān)Roger Perlmutter甚至要求手下的項(xiàng)目團(tuán)隊(duì)解釋為什么把預(yù)算韻給其它新項(xiàng)目,而不是繼續(xù)追加pembrolizumab的投入。結(jié)果是pembrolizumab果真在美贏得首創(chuàng)PD-1抑制劑地位。那么這是否說(shuō)明Keytruda能保持在黑色素瘤疾病領(lǐng)域的領(lǐng)先地位,和其它同類產(chǎn)品相比贏得主要的銷售份額呢?下面作者以美國(guó)黑色素瘤市場(chǎng)為例,簡(jiǎn)單介紹現(xiàn)行黑色素瘤的標(biāo)準(zhǔn)療法,解釋Keytruda和現(xiàn)行標(biāo)準(zhǔn)相比的優(yōu)勢(shì)和潛力所在,并分析和其它在研產(chǎn)品相比的競(jìng)爭(zhēng)力。
黑色素瘤(melanoma)在中國(guó)很罕見,即使在美國(guó)也是較少見的一類皮膚癌。黑色素瘤惡性較高,如果發(fā)現(xiàn)得晚死亡率非常高。據(jù)保守估算,美國(guó)2014年新增黑色素瘤病例大約7萬(wàn)6千人,死亡人數(shù)估計(jì)9710人。而且黑色素瘤的發(fā)病率繼續(xù)攀高,增幅尤其在男性中居所有癌癥發(fā)病率之首。與其他惡性腫瘤一樣,黑色素瘤的預(yù)后取決于初始診斷時(shí)的分期,其中局部型(AJCC Ⅰ或Ⅱ期)在美國(guó)新診斷患者中占82-85%、區(qū)域轉(zhuǎn)移型(AJCC Ⅲ期)占10-13%、遠(yuǎn)程轉(zhuǎn)移(AJCC Ⅳ期)的患者占2-5%。腫瘤厚度小于1毫米的局部型病變患者預(yù)后良好,5年生存率的患者數(shù)超過90%。但遠(yuǎn)程轉(zhuǎn)移黑色素瘤患者的預(yù)后非常低,長(zhǎng)期生存率通常小于10%。當(dāng)然也不排除一些患者因生物學(xué)特性獨(dú)特而進(jìn)展緩慢的個(gè)案。
在2011年之前,早在1975就獲得美國(guó)FDA批準(zhǔn)上市的老藥—達(dá)卡巴嗪(Dacarbazine)化療是治療轉(zhuǎn)移性黑色素瘤的主要手段。達(dá)卡巴嗪是DNA烷基化類細(xì)胞毒素,不僅副作用大,而且應(yīng)答率只有10%左右,1年生存率只有36%。自2011年以來(lái),美國(guó)FDA在Keytruda之前批準(zhǔn)了ipilimumab(2011)、聚乙二醇干擾素α-2B(2011)、vemurafenib(2011)、dabrafenib(2013)、和trametinib(2013)等5個(gè)黑色素瘤新藥上市,明顯改善了黑色素瘤的治療現(xiàn)狀。其中施貴寶的Yervoy(通用名:ipilimumab)是抗細(xì)胞毒性T淋巴細(xì)胞抗原4(CTLA4)的單克隆抗體,雖然Yervoy和達(dá)卡巴嗪相比的應(yīng)答率改善不大,但能明顯改善患者的總生存期。Zelboraf(通用名:Vemurafenib)和Tafinlar(dabrafenib)是小分子BRAF抑制劑,能把BRAF V600基因突變患者的應(yīng)答率提高到百分之五十以上,總生存期也有所延長(zhǎng)。Mekinist(通用名:trametinib)是首創(chuàng)MEK抑制劑,雖然Mekinist單藥治療的應(yīng)答率只有22%,但Tafinlar和Mekinist的復(fù)方組合能把應(yīng)答率提高到67%,在今年1月獲得FDA的批準(zhǔn)上市。但遺憾的是采用后三種小分子抗腫瘤藥治療后通常產(chǎn)生耐藥性。下表列出NCCN最新版(2014年第4版)指南治療轉(zhuǎn)移性或不可手術(shù)的黑色素瘤患者的優(yōu)選和替代系統(tǒng)治療方案。
表1、NCCN最新版(2014年第4版)指南治療轉(zhuǎn)移性或不可手術(shù)的黑色素瘤患者的系統(tǒng)療法。
|
治療方案
|
用藥方案
(商品名)
|
作用機(jī)理
|
適用范圍
|
備注
|
參考文獻(xiàn)
|
|
優(yōu)選方案
|
Ipilimuab(Yervoy)
|
CTLA4抑制劑
|
野生型或BRAF基因突變型
|
Ipilimumab能導(dǎo)致免疫介導(dǎo)的并發(fā)癥。未出現(xiàn)嚴(yán)重系統(tǒng)毒性以及臨床應(yīng)答后復(fù)發(fā),或病情穩(wěn)定3月后進(jìn)展的患者可再次使用。
|
1
|
|
Vemurafenib(Zelboraf)
|
BRAF抑制劑
|
B-RAF基因V600突變
|
僅適用于采用FDA或CLIA認(rèn)證的伴隨試劑盒檢測(cè)B-RAF基因V600突變的患者。Vemurafenib能引起包括皮膚鱗狀細(xì)胞癌、極端光過敏等皮膚并發(fā)癥。患者給藥后必須定期接受檢查并報(bào)告其它不良反應(yīng)。
|
2
|
|
|
Debrafenib(Tafinlar)
|
BRAF抑制劑
|
B-RAF基因V600突變
|
僅適用于采用FDA或CLIA認(rèn)證的伴隨試劑盒檢測(cè)B-RAF基因V600突變的患者。Dabrafenib能引起復(fù)發(fā)性高燒,出現(xiàn)后立即停止用藥并使用乙酰氨基酚或NSAIDs等退燒藥緩解。Dabrafenib還能引起角化棘皮瘤、早期的鱗狀細(xì)胞癌、和微弱的光敏感。患者給藥后必須定期接受健康檢查并報(bào)告其它包括關(guān)節(jié)腫脹和疼痛等不良反應(yīng)。
|
3
|
|
|
Debrafenib和trametinib復(fù)方組合
|
BRAF和MEK抑制劑
|
B-RAF基因V600突變
|
僅適用于采用FDA或CLIA認(rèn)證的伴隨試劑盒檢測(cè)B-RAF基因V600突變的患者。和dabrafenib單藥治療相比,dabrafenib和trametinib聯(lián)合治療在早中期臨床研究中改善無(wú)進(jìn)展生存期(PFS),但對(duì)總生存期的影響沒有確定。聯(lián)合用藥和單方治療相比皮膚毒性降低。
|
4
|
|
|
高劑量IL-2
|
化療方案
|
野生型或BRAF基因突變型
|
高劑量IL-2不適用臟器功能貯備不足、性能較差、未治療或表現(xiàn)活性癥狀的腦轉(zhuǎn)移患者。對(duì)于腦轉(zhuǎn)移灶較小或沒有瘤周水腫的患者,IL-2治療可以考慮。多藥聯(lián)合以及高劑量IL-2的應(yīng)用十分復(fù)雜,可引起嚴(yán)重的毒性反應(yīng),需要在有經(jīng)驗(yàn)的臨床醫(yī)師指導(dǎo)下進(jìn)行治療。
|
5
|
|
|
臨床實(shí)驗(yàn)
|
不詳
|
不詳
|
不詳
|
||
|
其它方案
|
Trametinib(Mekinist)
|
MEK抑制劑
|
B-RAF基因V600突變
|
僅適用于采用FDA或CLIA認(rèn)證的伴隨試劑盒檢測(cè)B-RAF基因V600突變的患者。Trametinib單藥治療不適用之前使用BRAF抑制劑治療但有進(jìn)展的患者。適用BRAF突變但對(duì)其它BRAF抑制劑不耐受的患者。
|
6
|
|
伊馬替尼
|
BCR-abl抑制劑
|
到目前為止美國(guó)FDA批準(zhǔn)了伊馬替尼的10種適應(yīng)癥,但不包括黑色素瘤
|
7
|
||
|
替莫唑胺
|
化療方案
|
盡管還沒有得到批準(zhǔn),但替莫唑胺經(jīng)常被醫(yī)生用于治療腦轉(zhuǎn)移的黑色素瘤患者。
|
8
|
||
|
達(dá)卡巴嗪
|
化療方案
|
野生型或BRAF基因突變型
|
轉(zhuǎn)移性黑色素瘤
|
9
|
|
|
Albumin-bound paclitaxel
|
化療方案
|
nab-paclitaxel
|
10
|
||
|
Paclitaxel
|
化療方案
|
11
|
|||
|
Paclitaxel + 順鉑
|
化療方案
|
13
|
|||
|
達(dá)卡巴嗪或替莫唑胺為基礎(chǔ)的聯(lián)合方案
|
化療方案
|
野生型或BRAF基因突變型
|
包括順鉑和春花堿加或不加IL-2,α-IFN),多藥聯(lián)合以及高劑量IL-2的應(yīng)用十分復(fù)雜,可引起嚴(yán)重的毒性反應(yīng),需要在有經(jīng)驗(yàn)的臨床醫(yī)師指導(dǎo)下進(jìn)行治療。
|
12
|
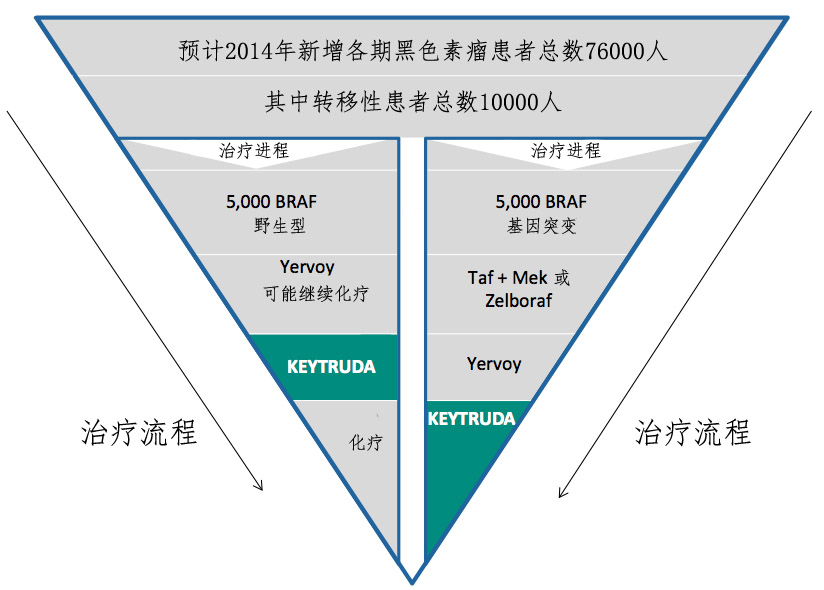
自9月4日Keytruda在美國(guó)獲得批準(zhǔn)上市以后,轉(zhuǎn)移性黑色素瘤的系統(tǒng)治療顯然又發(fā)生了變化,盡管這個(gè)變化還沒有反映在最新版的NCCN指南上。下圖簡(jiǎn)單闡明轉(zhuǎn)移性黑色素瘤治療的最新治療流程。
預(yù)計(jì)2014年新診斷的7萬(wàn)6千黑色素瘤患者中大約有1萬(wàn)患者是轉(zhuǎn)移性的,其中野生型或帶有BRAF V600基因突變的患者大約各占一半。經(jīng)FDA或CLIA認(rèn)證試劑盒檢測(cè)有BRAF V600基因突變患者的優(yōu)選方案有Zelboraf、Tafinlar和Mekinist復(fù)方組合,并且包括和Yervoy的聯(lián)合治療。野生型患者的一線療法主要有Yervoy,包括有或沒有后續(xù)的化療。Keytruda作為二線或三線療法被批準(zhǔn)用于治療已經(jīng)接受過ipilimumab治療但仍有進(jìn)展,或?qū)RAF V600基因變異的患者依序經(jīng)過BRAF抑制劑和ipilimumab治療但顯示耐藥的患者。據(jù)Leerink估計(jì),根據(jù)默克每位患者每月12500美元的價(jià)格,Keytruda的年銷售額預(yù)計(jì)在1億4千萬(wàn)美元左右。
雖然nivolumab(商品名:Opdivo)直到明年夏天才能獲得FDA的上市許可,但有望允許作為一線用藥使用,占據(jù)上圖Yervoy的位置或者和Yervoy聯(lián)合使用。而2013年Yervoy的全球銷售額高達(dá)5.77億美元。也就是說(shuō)Opdivo雖然未能作為首創(chuàng)PD-1抑制劑上市,但適用范圍的起點(diǎn)超過Keytruda。當(dāng)然,Keytruda作為率先上市的PD-1抑制劑,醫(yī)生對(duì)那些的嚴(yán)重患者也會(huì)考慮優(yōu)先采用Keytruda治療(off-label use),有時(shí)這部分的銷售額也會(huì)很高,增加了了Keytruda的市場(chǎng)份額。
目前Opdivo在日本的售價(jià)是每位患者每年14萬(wàn)3千美元,一些分析人士指出如果Opdivo明年在美上市,售價(jià)會(huì)略低于目前在日本的價(jià)格,大約每年11萬(wàn)美元左右。如果Opdivo上市后能迅速取代Yervoy,處方數(shù)有望超過2000,這樣在美國(guó)的年銷售額即將超過2億美元。當(dāng)然Opdivo是否能趕超Keytruda還取決于后者開發(fā)作為一線用藥的進(jìn)度,無(wú)論如何默克為Keytruda所做的努力已經(jīng)得到回報(bào),至少已經(jīng)獲得能和最初領(lǐng)先的PD-1抑制劑nivolumab市場(chǎng)上一決雌雄的本錢。
參考文獻(xiàn):
1、 (i)Margolin K, Ernstoff MS, Hamid O, et al. Ipilimumab in patients with melanoma and brain metastases: an open-label, phase 2 trial. Lancet Oncol 2012;13:459-465. (ii) Weber JS, Kahler KC, Hauschild A. Management of Immune-Related Adverse Events and Kinetics of Response With Ipilimumab. J Clin Oncol 2012. (iii) Hodi FS, O’Day SJ, McDermott DF, Weber RW, et al. Improved survival with ipilimumab in patients with metastatic melanoma. N Eng J Med 2010;363:711-723. (iv) Robert C, Thomas L, Bondarenko I, et al. Ipilimumab plus dacarbazine for previously untreated metastatic melanoma. N Engl J Med 2011;364:2517-2526.
2、 (i)Sosman JA, Kim KB, Schuchter L, et al. Survival in BRAF V600-mutant advanced melanoma treated with vemurafenib. N Engl J Med 2012;366:707-714. (ii) Chapman PB, Hauschild A, Robert C, et al. Improved survival with vemurafenib in melanoma with BRAF V600E mutation. N Engl J Med 2011;2507-2516.
3、 Hauschild A, Grob JJ, Demidov LV, et al. Dabrafenib in BRAFmutated metastatic melanoma: a multicentre, open-label, phase 3 randomised controlled trial. Lancet 2012;380:358-365.
4、 Flaherty KT, Infante JR, Daud A, et al. Combined BRAF and MEK Inhibition in Melanoma with BRAF V600 Mutations. N Eng J Med 2012;367:1694-1703.
5、 (i) Rosenberg SA, Yang JC, Topalian SL, et al. Treatment of 283 consecutive patients with metastatic melanoma or renal cell cancer using high-dose bolus interleukin 2. JAMA 1994;271:907-913. (ii) Atkins MB, Lotze MT, Dutcher JP, et al. High-dose recombinant interleukin 2 therapy for patients with metastatic melanoma: analysis of 270 patients treated between 1985 and 1993. J Clin Oncol 1999;17:2105-2116. (iii) Atkins MB, Kunkel L, Sznol M, Rosenberg SA. High-dose recombinant interleukin-2 therapy in patients with metastatic melanoma: long-term survival update. Cancer J Sci Am 2000;6 Suppl 1:S11-14. (iv) Smith FO, Downey SG, Klapper JA, et al. Treatment of metastatic melanoma using interleukin-2 alone or in conjunction with vaccines. Clin Cancer Res 2008;14(17):5610-5618.
6、 Flaherty KT, Robert C, Hersey P, et al. Improved Survial with MEK Inhibition in BRAF-mutated melanoma. N Eng J Med 2012;367:107-114.
7、 Carvajal RD, Antonescu CR, Wolchok, JD, et al. KIT as a therapeutic target in metastatic melanoma. JAMA 2011;395:2327-2334.
8、 Middleton MR, Grob JJ, Aaronson N, et al. Randomized phase III study of temozolomide versus dacarbazine in the treatment of patients with advanced metastatic malignant melanoma. J Clin Oncol 2000;18:158-166.
9、 Serrone L, Zeuli M, Sega FM, et al. Dacarbazine-based chemotherapy for metastatic melanoma: thirty-year experience overview. J Exp Clin Cancer Res 2000;19:21-34.
10、 Hersh EM, O'Day SJ, Ribas A, et al. A phase 2 Clinical trial of nab-Paclitaxel in previously treated and chemotherapy-na?ve patients with metastatic melanoma. Cancer 2010;116:155-163. (ii) Kottschade LA, Suman VJ, Amatruda T, et al. A phase II trial of nab-paclitaxel (ABI-007) and carboplatin in patients with unresectable stage iv melanoma: a north central cancer treatment group study, N057E(1). Cancer 2011;117:1704-1710.
11、 Wiernik PH and Einzig AI. Taxol in malignant melanoma. J Natl Cancer Inst Monogr 1993;15:185-187.
12、 (i) Legha SS, Ring S, Eton O, et al. Development of a biochemotherapy regimen with concurrent administration of cisplatin, vinblastine, dacarbazine, interferon alfa, and interleukin-2 for patients with metastatic melanoma. J Clin Oncol 1998;16:1752-1759. (ii) Eton O, Legha SS, Bedikian AY, et al. Sequential biochemotherapy versus chemotherapy for metastatic melanoma: results from a phase III randomized trial. J Clin Oncol 2002;20:2045-2052. (iii) O'Day SJ, Boasberg PD, Piro L, Kristedja TS, et al. Maintenance biotherapy for metastatic melanoma with interleukin-2 and granulocyte macrophagecolony stimulating factor improves survival for patients responding to induction concurrent biochemotherapy. Clin Cancer Res. 2002(9):2775-2781. (iv) Ives NJ, Stowe RL, Lorigan P, Wheatley K. Chemotherapy compared with biochemotherapy for the treatment of metastatic melanoma: a metaanalysis of 18 trials involving 2,621 patients. J Clin Oncol 2007 25(34):5426-5434. (v) Atkins MB, Hsu J, Lee S, et al. Phase III trial comparing concurrent biochemotherapy with cisplatin, vinblastine, dacarbazine, interleukin-2, and interferon alfa-2b with cisplatin, vinblastine, and dacarbazine alone in patients with metastatic malignant melanoma (E3695): a trial coordinated by the eastern cooperative oncology group. J Clin Oncol 2008 Dec 10; 26(35):5746-5754.
13、 (i) Rao RD, Holtan SG, Ingle JN, et al. Combination of paclitaxel and carboplatin as second-line therapy for patients with metastatic melanoma. Cancer. 2006;106(2):375-382. (ii) Agarwala SS, Keilholz U, Hogg D, et al. Randomized phase III study of paclitaxel plus carboplatin with or without sorafenib as second-line treatment in patients with advanced melanoma. J Clin Oncol (Meeting Abstracts). 2007;25(18_suppl):8510. (iii) Hauschild A, Agarwala SS, Trefzer U, et al. Results of a phase III, randomized, placebo-controlled study of sorafenib in combination with carboplatin and paclitaxel as second-line treatment in patients with unresectable stage III or stage IV melanoma. J Clin Oncol 2009;27:2823-2830. (iv) Flaherty KT, Lee SJ, Schuchter LM, et al. Final results of E2603: A double-blind, randomized phase III trial comparing carboplatin. (C)/paclitaxel (P) with or without sorafenib (S) in metastatic melanoma. J Clin Oncol (ASCO Meeting Abstracts) 2010. 28:(suppl; abstr):8511.
★更多深度解析訪問《美中藥源》~
★ 請(qǐng)關(guān)注《美中藥源》微信公眾號(hào) ★

發(fā)表評(píng)論
要發(fā)表評(píng)論,您必須先登錄。


















 微信號(hào):美中藥源
微信號(hào):美中藥源