
2019年FDA批準(zhǔn)48款新藥、高調(diào)結(jié)束了21世紀(jì)第二個(gè)10年。這10年是制藥工業(yè)復(fù)蘇的10年,不僅新藥產(chǎn)出數(shù)量遠(yuǎn)超第一個(gè)10年、而且很多新技術(shù)進(jìn)入成熟期。基因療法、細(xì)胞療法、RNAi、ASO、雙特異抗體、ADC這些2009年時(shí)還是科幻或非主流的技術(shù)現(xiàn)在已經(jīng)都有不止一個(gè)藥物上市,基因編輯、蛋白降解等當(dāng)時(shí)做夢(mèng)也想不到的技術(shù)也已經(jīng)開始了人體臨床試驗(yàn)。
Continue reading …
今天美國(guó)聯(lián)邦貿(mào)易委員會(huì)(FTC)宣布經(jīng)過10個(gè)月調(diào)查,沒有證據(jù)表明羅氏收購(gòu)Spark會(huì)減慢或終止Spark的A型血友病基因療法的開發(fā),也不會(huì)影響羅氏自己F8模擬物、雙特異抗體Hemlibra的可及性。FTC驚奇地發(fā)現(xiàn)Spark只是開發(fā)血友病基因療法公司之一,這個(gè)收購(gòu)不僅不會(huì)減慢這些藥物的開發(fā)、反而因?yàn)榕c其它廠家競(jìng)爭(zhēng)會(huì)加速。
Continue reading …
今天日本制藥巨頭安斯泰來宣布將以每股60美元、總值30億美元收購(gòu)美國(guó)基因療法公司Audentes,這個(gè)價(jià)格相當(dāng)于昨天收盤價(jià)溢價(jià)110%。
Continue reading …
今天Incyte宣布FDA接受了其FGFR抑制劑pemigatinib在FGFR2融合或易位晚期膽管癌二線以后治療的上市申請(qǐng)。在一個(gè)叫做FIGHT-202的二期臨床試驗(yàn)中pemigatinib在這個(gè)人群產(chǎn)生36%應(yīng)答率、中位應(yīng)答時(shí)間為7.5個(gè)月。
Continue reading …
今天麻省總醫(yī)院和哈佛大學(xué)科學(xué)家在《Cell Reports》發(fā)表一項(xiàng)工作,評(píng)價(jià)老藥色甘酸鈉在SOD1變異(G93A)驅(qū)動(dòng)小鼠ALS模型的療效。作者發(fā)現(xiàn)腹腔注射色甘酸鈉可以顯著推遲ALS癥狀出現(xiàn)(20小鼠天,相當(dāng)于人的10年)、增加小鼠肌肉功能(根據(jù)一個(gè)叫做PaGE 的指標(biāo))、并延長(zhǎng)雌性小鼠壽命(但對(duì)雄性無(wú)影響)。表征上色甘酸鈉緩解肌肉去神經(jīng)、改善運(yùn)動(dòng)神經(jīng)元生存、并降低炎癥細(xì)胞因子水平。
Continue reading …
今天FDA批準(zhǔn)了Global Blood Therapeutics, Inc. (GBT)的小分子鐮刀細(xì)胞疾病(SCD)藥物Oxbryta (通用名voxeloto,曾用名GBT440) 用于12歲以上患者的治療。
Continue reading …
Alnylam的Givosiran(商品名Givlaari)今天被FDA批準(zhǔn)用于一種叫做急性肝卟啉病(AHP)的超級(jí)罕見病,成為第二個(gè)在美國(guó)上市的RNAi藥物。這個(gè)批準(zhǔn)是根據(jù)一個(gè)叫做ENVISION的三期臨床試驗(yàn),
Continue reading …
今天FDA通過加速審批通道批準(zhǔn)了百濟(jì)神州的BTK抑制劑Brukinsa (通用名zanubrutinib)用于治療至少失敗一種療法的套細(xì)胞淋巴瘤。這個(gè)審批是根據(jù)一個(gè)86人參與的單臂臨床試驗(yàn)結(jié)果,Brukinsa在這個(gè)人群的應(yīng)答率為84%、中值應(yīng)答時(shí)間為19.5個(gè)月。
Continue reading …
今天諾華SMN1基因療法Zolgensma的兩個(gè)臨床試驗(yàn)被FDA部分叫停。一個(gè)叫做STRONG的臨床試驗(yàn)低劑量組已經(jīng)結(jié)束、將停止招募和使用高劑量Zolgensma。
Continue reading …
今天FDA批準(zhǔn)了福泰的囊腫性肺纖維化(CF)三藥組合Trikafta(elexacaftor, tezacaftor,ivacaftor)用于12歲以上、CFTR至少有一種F508del型變異的CF患者。這個(gè)審批是根據(jù)兩個(gè)三期臨床的陽(yáng)性結(jié)果,
Continue reading …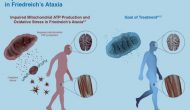
今天美國(guó)生物技術(shù)公司Reata宣布其Nrf2激活劑Omaveloxolone在一個(gè)叫做MOXIe 的 弗里德賴希共濟(jì)失調(diào)(FA)二期臨床試驗(yàn)的注冊(cè)部分達(dá)到試驗(yàn)終點(diǎn)。
Continue reading …
據(jù)《State News》報(bào)道美國(guó)一個(gè)叫做Tremeau Pharmaceuticals 的生物技術(shù)公司正在開發(fā)默沙東原COX2抑制劑萬(wàn)絡(luò)(通用名羅非昔布)的一個(gè)仿制藥產(chǎn)品TRM - 201,準(zhǔn)備用于血友病患者因關(guān)節(jié)淤血而導(dǎo)致的血友病性關(guān)節(jié)病。萬(wàn)絡(luò)曾經(jīng)是個(gè)非常受歡迎的關(guān)節(jié)炎止痛藥物,也被醫(yī)生標(biāo)簽外使用用于血友病性關(guān)節(jié)病,所以療效基本可以保證。Tremeau也在開發(fā)默沙東另一個(gè)COX2抑制劑Arcoxia的仿制藥。
Continue reading …
今天美國(guó)mRNA技術(shù)公司Moderna公布了兩個(gè)mRNA產(chǎn)品的一期臨床數(shù)據(jù)。一個(gè)產(chǎn)品是巨細(xì)胞病毒(CMV)疫苗mRNA-1647。這個(gè)產(chǎn)品共有6段mRNA,其中五條編碼膜上的5個(gè)亞單位、第六條編碼糖蛋白B。
Continue reading …
今天只有4年歷史的IFM宣布其子公司IFM Due獲得諾華未公布數(shù)目的研發(fā)支持和總值可達(dá)8.4億美元的收購(gòu)選擇。IFM Due今年2月才成立,主要研究方向是cGAS/STING拮抗劑,
Continue reading …
今天FDA批準(zhǔn)了新基的JAK2抑制劑fedratinib(商品名Inrebic)用于治療原發(fā)、繼發(fā)性骨髓纖維化。在一個(gè)叫做JAKARTA的三期臨床試驗(yàn)中,每天 400毫克Inrebic 令37%患者縮小至少35%脾臟體積、而安慰劑組只有1%患者達(dá)到這個(gè)水平。
Continue reading …
今天再生元宣布其ANGPTL3抗體evinacumab在一個(gè)三期臨床顯示強(qiáng)力降脂療效。這個(gè)叫做ELIPSE HoFH的臨床試驗(yàn)招募65位純合家族性高血脂癥患者(HoFH)
Continue reading …
今天FDA發(fā)表公告稱諾華的SMA1基因療法Zolgensma上市申請(qǐng)材料有造假嫌疑。今年FDA批準(zhǔn)這個(gè)史上最貴藥物一個(gè)月后諾華旗下AveXis通知FDA該藥物申請(qǐng)中部分動(dòng)物實(shí)驗(yàn)數(shù)據(jù)不實(shí)
Continue reading …
今天BioMarin宣布將利用其A型血友病基因療法Valrox的一/二期臨床數(shù)據(jù)和部分三期臨床數(shù)據(jù)在今年年底申請(qǐng)加速審批上市。
Continue reading …


















 微信號(hào):美中藥源
微信號(hào):美中藥源