
今天諾和諾德宣布其GLP激動劑索瑪魯肽在一個(gè)NASH二期臨床達(dá)到一級終點(diǎn)。這個(gè)試驗(yàn)招募320位1-3級NASH患者,分別使用0.1、0.2、0.4毫克一日一次皮下注射索瑪魯肽和安慰劑。
Continue reading …
昨天阿斯列康宣布其P2Y12受體拮抗劑倍林達(dá)在一個(gè)叫做THALES的大型三期臨床達(dá)到臨床終點(diǎn)。這個(gè)試驗(yàn)招募11,000位微中風(fēng)或高危移過性中風(fēng)
Continue reading …
今天FDA批準(zhǔn)了AMRN純EPA魚油制劑Vascepa標(biāo)簽擴(kuò)展申請,現(xiàn)在有心血管病史、無心血管病史但有糖尿病加另外兩種心血管疾病風(fēng)險(xiǎn)因素的患者
Continue reading …
今天制藥巨頭賽諾菲新掌門人Paul Hudson宣布了其執(zhí)政綱領(lǐng),主要戰(zhàn)略變更是退出糖尿病、心血管疾病的研發(fā),因此將節(jié)省約22億歐元的研發(fā)開支。已經(jīng)上市產(chǎn)品將并入通用藥物部門,按成熟產(chǎn)品經(jīng)營。
Continue reading …
今天Bloomberg News報(bào)道諾華可能收購開發(fā)PCSK9 RNAi藥物inclisiran的Medicines Company,令今天MDCO股票上揚(yáng)20%。
Continue reading …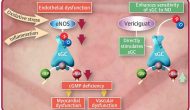
今天默沙東與合作伙伴拜耳宣布其心衰藥物、可溶性鳥苷酸環(huán)化酶(sGC)激動劑Vericiguat在一個(gè)叫做VICTORIA的國際多中心三期臨床試驗(yàn)達(dá)到由心衰住院和心血管死亡組成的復(fù)合一級終點(diǎn)。
Continue reading …
昨天FDA專家組以16:0全票支持將Amarin的純EPA魚油制劑Vascepa標(biāo)簽擴(kuò)展到心血管預(yù)防,礦物油作為安慰劑并未令專家組質(zhì)疑關(guān)鍵試驗(yàn)Reduce-it結(jié)果的可靠性,但專家對是否將標(biāo)簽限制在二級預(yù)防、出血和心率不齊危險(xiǎn)等進(jìn)行了討論。
Continue reading …
今天FDA批準(zhǔn)了諾和諾德的口服GLP激動劑索瑪魯肽(商品名Rybelsus)用于二型糖尿病患者血糖控制。這個(gè)批準(zhǔn)是根據(jù)10個(gè)三期臨床共約10,000患者的試驗(yàn)結(jié)果,包括單方與安慰劑、
Continue reading …
正在進(jìn)行的歐洲心臟病協(xié)會年會(ESC)上公布了幾個(gè)重要產(chǎn)品的晚期臨床結(jié)果。其中Medicines Company的RNAi藥物inclisiran的Orion-11結(jié)果最引人注目,半年一次inclisiran令患者LDL-C下降54%、并且在相對虛弱的CVD患者中沒有出現(xiàn)嚴(yán)重毒副反應(yīng),
Continue reading …
今天Medicines Company公布了其PCSK9 RNAi藥物inclisiran一個(gè)關(guān)鍵三期臨床的頂層數(shù)據(jù)分析結(jié)果,這個(gè)叫做ORION-11的三期臨床招募1,617位有心血管風(fēng)險(xiǎn)(ASCVD)、最高劑量他汀無法有效控制LDL-C的高血脂患者,
Continue reading …
今天阿斯列康宣布其SGLT2抑制劑Farxiga(通用名dapagliflozin) 在一個(gè)叫做DAPA-HF的心衰三期臨床試驗(yàn)中達(dá)到一級終點(diǎn)。這個(gè)試驗(yàn)招募4744位左心室射血不足心衰(HFrEF)患者,
Continue reading …
今天再生元宣布其ANGPTL3抗體evinacumab在一個(gè)三期臨床顯示強(qiáng)力降脂療效。這個(gè)叫做ELIPSE HoFH的臨床試驗(yàn)招募65位純合家族性高血脂癥患者(HoFH)
Continue reading …
今天諾華宣布其慢性心衰藥物Entresto在一個(gè)叫做PARAGON-HF的三期臨床錯過由死亡和心衰導(dǎo)致總住院次數(shù)組成的復(fù)合一級終點(diǎn)。
Continue reading …






















 微信號:美中藥源
微信號:美中藥源