
FDA優(yōu)先審評券(priority review voucher,PRV)問答
2007年以來FDA發(fā)放了少量的優(yōu)先審評券。一張優(yōu)先審評券可以令使用者加快任何一個FDA新藥申報的審評,從標準的10個月審評時間縮短至優(yōu)先評審的6個月。

在美國密歇根執(zhí)業(yè)的腫瘤醫(yī)生法里得?法塔(Farid Fata)從6日開始在底特律法庭接受審判,他被控涉及違反醫(yī)療法,惡意欺騙病人稱他們患有癌癥,然后對其進行不必要的化療,從中牟取暴利。
Continue reading …
本周四FDA專家組將討論禮來EGFR抗體necitumumab的上市申請。Necitumumab的申請適應癥為與化療聯(lián)用作為晚期鱗狀非小細胞肺癌的一線用藥。
Continue reading …福泰制藥Orkambi獲得美國FDA批準,治療F508del突變的囊性纖維化(CF)
2015年7月3日 福泰制藥Orkambi獲得美國FDA批準,治療F508del突變的囊性纖維化(CF)已關閉評論
美國FDA今天批準了福泰制藥的Orkambi,用于治療12歲或以上的帶有F508del基因變異的囊性纖維化患者。
Continue reading …
美國司法部因為諾華支付回扣的促銷行為違反了美國《虛假申報法》(False Claims Act),今日向紐約聯(lián)邦法院訴其醫(yī)療欺詐。要求諾華除了支付因醫(yī)療欺詐給聯(lián)邦政府帶來的損失之外,再額外處罰罰金共33.5億美元。
Continue reading …
6月29日,西班牙PharmaMar制藥公司的抗癌實驗藥PM1183(lurbinectedin)的一個3期臨床(NCT02421588)注冊了第一個病人。6月27日,浙江中醫(yī)藥大學宣布美國FDA同意其抗癌中藥康萊特注射液進入3期臨床研究,治療晚期胰腺癌。
Continue reading …
上周瑞士大佬Ernesto Bertarelli成立一個擁有20億美元資本,名為Gurnet的生物技術投資公司,由賽諾菲前CEO Chris Viehbacher 掛帥。
Continue reading …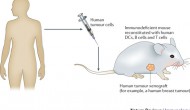
缺乏明顯療效是新藥開發(fā)失敗的最重要原因。雖然動物和人,疾病模型和疾病本身有著巨大區(qū)別,但實驗動物模型依然是預測后期臨床療效,降低臨床開發(fā)風險的最重要步驟之一。
Continue reading …
最近網(wǎng)上吵吵嚷嚷的一項大型臨床研究指出,服用“偉哥”等5型磷酸二酯酶(PDE5)抑制劑類藥物的男士,罹患一種叫黑色素瘤的皮膚癌風險和一般人相比要高出21%。更有一些文章以“要man還是要命?偉哥或增加男性皮膚癌風險”等為醒目標題,致使服用這類藥物的一些男士憂心忡忡。
Continue reading …生命不再無價:美國臨床腫瘤協(xié)會(ASCO)發(fā)布抗癌藥“價值框架”(value framework)
2015年6月25日 生命不再無價:美國臨床腫瘤協(xié)會(ASCO)發(fā)布抗癌藥“價值框架”(value framework)已關閉評論
一個由哈佛大學Lowell E. Schnipper教授為組長的美國臨床腫瘤協(xié)會(ASCO)工作組6月22日在美國《臨床腫瘤雜志》(Journal of Clinical Oncology)上在線發(fā)表了一個為抗癌藥打分的“評分指南”。
Continue reading …十年砥礪終成正果:美國FDA批準了Medicine’s Company的注射抗凝藥Cangrelor(Kengreal)上市
2015年6月23日 十年砥礪終成正果:美國FDA批準了Medicine’s Company的注射抗凝藥Cangrelor(Kengreal)上市已關閉評論
今天美國FDA批準了Medicine’s Company的抗血小板注射劑cangrelor上市(商品名:Kengreal),用于避免成人患者在經(jīng)皮冠狀動脈介入治療(percutaneous coronary intervention,PCI)過程中因凝血造成的冠狀動脈堵塞。
Continue reading …
上周《Nat. Rev. Drug Discov.》一篇分析顯示設計符合類藥性(drug-like)規(guī)則的候選藥物并不能真正增加這些藥物在開發(fā)路程上的成功率。那么現(xiàn)在藥物需要如何設計才能保證一定的成功率呢?
Continue reading …
最近總部位于紐約的一個公益性組織—Initiative for Medicines, Access & Knowledge(簡稱I-MAK)公布中國國家專利部門拒絕了吉利德科學的抗丙肝明星Sovaldi(通用名:sofosbuvir,索菲布韋)的一項重要前藥專利申請。雖然這個消息還沒有得到國家知識產(chǎn)權局或吉利德科學的證實,
Continue reading …
今天《Nature Reviews Drug Discovery》發(fā)表一篇由阿斯列康、禮來、葛蘭素、和輝瑞聯(lián)合發(fā)表的一篇文章。他們分析了四個公司在2000-2010年這10年間通過臨床前研究準備進入臨床開發(fā)812個藥物的命運,試圖通過計算藥物的理化性質來預測其成功率。到分析時已有605個化合物因為各種原因停止了開發(fā)。
Continue reading …
近期葛蘭素腫瘤免疫療法負責人Axel Hoos說抗腫瘤依然是葛蘭素的戰(zhàn)略重點之一,并透露正在積極進行OX40和與IDO類似的免疫微環(huán)境調(diào)節(jié)藥物研發(fā)。
Continue reading …
今天Evaluate Pharma發(fā)表的最新分析顯示今后5年全球處方藥銷量將以平均每年4.8%的速度增長,到2020年將達到9870億美元。諾華仍然會是最大的處方藥公司,現(xiàn)在在研藥物價值最高的是吉利德科學的丙肝藥物三方組合,作價248億美元。
Continue reading …阿斯列康痛風藥物Lesinurad三期臨床錯過一級終點,2023年450億美元銷售目標再受挑戰(zhàn)
2015年6月16日 阿斯列康痛風藥物Lesinurad三期臨床錯過一級終點,2023年450億美元銷售目標再受挑戰(zhàn)已關閉評論
今天阿斯列康在歐洲抗風濕病年會上公布其痛風藥物Lesinurad在一個叫做CRYSTAL的三期臨床實驗結果。在這個有324人參加、持續(xù)一年的實驗中,病人使用200毫克或400毫克Lesinurad與武田的非布索坦(80毫克)聯(lián)用和單獨使用非布索坦比較。只有400毫克組顯示尿酸控制在5毫克/分升以下的人數(shù)統(tǒng)計顯著超過對照組,而準備報批的200毫克劑量沒有顯示附加療效,因此錯過實驗一級終點。
Continue reading …
昨天一個叫做Axovant Science的制藥公司在美國上市,募集了3.15億美元,據(jù)說是生物制藥史上募資最多的IPO。最近生物制藥公司沒有產(chǎn)品線也能成功IPO已經(jīng)不是新聞,但這個公司即使在2015屆生物制藥企業(yè)中也是一朵奇葩。
Continue reading …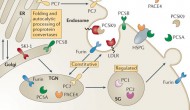
昨天FDA的分泌與代謝藥物顧問小組以13票贊成、3票反對的壓倒性結果支持賽諾菲的Praluent上市,今天幾乎是同一班人馬又以大致相同的投票結果(11票贊成、4票反對)支持安進的PCSK9抑制劑Repatha上市,其中全票(15:0)支持用于治療家族性高血脂癥患者。
Continue reading …
今天FDA專家組以13票贊成、3票反對的投票結果支持賽諾菲/再生元的PCSK9抑制劑Praluent上市,明天將討論安進的同類藥物。雖然Praluent獲得壓倒性支持,但適用人群至少暫時不會太大。
Continue reading …

















 微信號:美中藥源
微信號:美中藥源