
Alnylam制藥公司在本周舉行的美國心臟學(xué)會(huì)年會(huì)上宣布,在兩個(gè)小型臨床試驗(yàn)中皮下注射一針其PCSK9 RNA干擾藥物ALN-PCS,半年以后受試者的低密度膽固醇水平和基線相比還低47%。除此之外其它致動(dòng)脈粥樣脂的水平也明顯下降。
Continue reading …
今天默沙東宣布其CETP抑制劑anacetrapib的大型三期臨床試驗(yàn)REVEAL經(jīng)最后一次中期分析顯示沒有因?yàn)榀熜枰崆敖K止。因?yàn)檫@是最后一次中期分析,所以REVEAL將繼續(xù)進(jìn)行直到2017年試驗(yàn)結(jié)束。
Continue reading …
在今天進(jìn)行的美國心臟病協(xié)會(huì)年會(huì)上由NIH資助的高血壓實(shí)驗(yàn)SPRINT結(jié)果正式公布,同時(shí)在NEJM上發(fā)表,并伴隨發(fā)表三篇評(píng)論,顯示業(yè)界對(duì)此實(shí)驗(yàn)的重視。
Continue reading …
今天葛蘭素宣布其p38抑制劑Losmapimod在一個(gè)急性冠脈綜合癥的大型三期臨床失敗。這個(gè)叫做LATITUDE-TIMI60的臨床設(shè)計(jì)有些特別,因?yàn)轱L(fēng)險(xiǎn)巨大這個(gè)總共有25000人參與的實(shí)驗(yàn)分三部分。今天失敗的是第一部分,共有3503人參與。
Continue reading …
美國生物技術(shù)公司Zafgen昨天臨時(shí)取消兩個(gè)投資者見面會(huì)并沒有給出任何理由,令投資者懷疑其主打產(chǎn)品metAP2抑制劑beloranib的臨床開發(fā)出了意外事故。Zafgen股票昨天下跌35%,今天繼續(xù)下跌19%,但公司依然沒有任何解釋,令投資者疑惑同時(shí)倍感憤怒。
Continue reading …
今天禮來宣布在對(duì)其CETP抑制劑Evacetrapib的CVOT三期臨床試驗(yàn)(ACCELERATE)進(jìn)行中期分析后決定停止該藥物的臨床開發(fā)。分析顯示Evacitrapib達(dá)到該試驗(yàn)臨床終點(diǎn)的機(jī)會(huì)很小。
Continue reading …
上個(gè)月Esperion宣布與FDA溝通后FDA認(rèn)為ETC1002在家族性高血脂和慢性動(dòng)脈硬化這兩個(gè)適應(yīng)癥不需要心血管實(shí)驗(yàn)結(jié)果即可上市,但今天卻宣布他們可能還需要CVOT才能上市。
Continue reading …
今天禮來和BI二型糖尿病藥物Jardiance的CVOT試驗(yàn)結(jié)果在EASD年會(huì)上正式公布。這個(gè)名為EMPA-REG的試驗(yàn)比較10毫克和25毫克Jardiance和安慰劑比較對(duì)全因死亡、心臟病死亡、非致死心梗、非致死中風(fēng)的影響。
Continue reading …
今天美國國立衛(wèi)生研究院資助的一個(gè)叫做Systolic Blood Pressure Intervention Trial (SPRINT)的臨床試驗(yàn)因?yàn)榀熜Ш糜陬A(yù)測而提前終止。正如試驗(yàn)名字所言這個(gè)試驗(yàn)研究控制收縮壓對(duì)死亡風(fēng)險(xiǎn)的影響。
Continue reading …
昨天葛蘭素宣布其COPD藥物Breo Ellipta(糠酸氟替卡松和維蘭特羅的復(fù)方組合)在一個(gè)叫做SUMMIT(意為登頂)的臨床試驗(yàn)中錯(cuò)過一級(jí)終點(diǎn)。在這個(gè)一萬六千多人參與的試驗(yàn)中Breo和安慰劑比較沒有降低全因死亡風(fēng)險(xiǎn)。
Continue reading …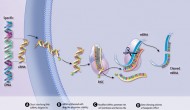
今天在歐洲心臟病協(xié)會(huì)年會(huì)上,Medicines Company公布了其PCSK9 RNA干擾(RNAi)藥物ALN-PCS的兩個(gè)小型臨床試驗(yàn)結(jié)果。
Continue reading …
今天FDA批準(zhǔn)了安進(jìn)的PCSK9抑制劑Repatha(通用名evolocumab)用于家族性高血脂癥和需要附加治療的高危動(dòng)脈硬化病人。這和賽諾菲/再生元的同類藥物Praluent的標(biāo)簽一樣。今天這個(gè)結(jié)果是大家基本預(yù)料到的,和FDA專家組的建議完全一致。PCSK9抑制劑的競爭和另一個(gè)激烈競爭領(lǐng)域PD-1抑制劑不太一樣。
Continue reading …
今天禮來和其合作伙伴BI宣布二型糖尿病藥物,SGLT2抑制劑Jardiance在一個(gè)名為EMPA-REG OUTCOME的前瞻性臨床試驗(yàn)中達(dá)到一級(jí)終點(diǎn)。在這個(gè)有7000多人參與的四期臨床試驗(yàn)中,平均跟蹤3.1年顯示Jardiance能延緩心梗、心臟病死亡、和中風(fēng)發(fā)病。
Continue reading …
今天美國生物技術(shù)公司Esperion公布其主打產(chǎn)品,降血脂藥物ETC1002的二期臨床進(jìn)展。重要的新聞是在和FDA溝通之后,F(xiàn)DA認(rèn)為在家族性高血脂和慢性動(dòng)脈硬化這兩個(gè)適應(yīng)癥ETC1002不需要心血管實(shí)驗(yàn)結(jié)果即可上市。
Continue reading …
今天FDA批準(zhǔn)了諾華的慢性心衰藥物Entresto(以前叫LCZ696),比PDUFA日期提前6周。Entresto是血管緊張素II抑制劑纈沙坦和腦啡肽酶抑制劑AHU-377的復(fù)方組合。這次批準(zhǔn)三個(gè)劑量(24/26,49/51,97/103毫克),標(biāo)簽為降低慢性心衰病人心臟病死亡和因心衰住院風(fēng)險(xiǎn)。
Continue reading …十年砥礪終成正果:美國FDA批準(zhǔn)了Medicine’s Company的注射抗凝藥Cangrelor(Kengreal)上市
2015年6月23日 十年砥礪終成正果:美國FDA批準(zhǔn)了Medicine’s Company的注射抗凝藥Cangrelor(Kengreal)上市已關(guān)閉評(píng)論
今天美國FDA批準(zhǔn)了Medicine’s Company的抗血小板注射劑cangrelor上市(商品名:Kengreal),用于避免成人患者在經(jīng)皮冠狀動(dòng)脈介入治療(percutaneous coronary intervention,PCI)過程中因凝血造成的冠狀動(dòng)脈堵塞。
Continue reading …阿斯列康痛風(fēng)藥物L(fēng)esinurad三期臨床錯(cuò)過一級(jí)終點(diǎn),2023年450億美元銷售目標(biāo)再受挑戰(zhàn)
2015年6月16日 阿斯列康痛風(fēng)藥物L(fēng)esinurad三期臨床錯(cuò)過一級(jí)終點(diǎn),2023年450億美元銷售目標(biāo)再受挑戰(zhàn)已關(guān)閉評(píng)論
今天阿斯列康在歐洲抗風(fēng)濕病年會(huì)上公布其痛風(fēng)藥物L(fēng)esinurad在一個(gè)叫做CRYSTAL的三期臨床實(shí)驗(yàn)結(jié)果。在這個(gè)有324人參加、持續(xù)一年的實(shí)驗(yàn)中,病人使用200毫克或400毫克Lesinurad與武田的非布索坦(80毫克)聯(lián)用和單獨(dú)使用非布索坦比較。只有400毫克組顯示尿酸控制在5毫克/分升以下的人數(shù)統(tǒng)計(jì)顯著超過對(duì)照組,而準(zhǔn)備報(bào)批的200毫克劑量沒有顯示附加療效,因此錯(cuò)過實(shí)驗(yàn)一級(jí)終點(diǎn)。
Continue reading …FDA專家組推薦安進(jìn)Repatha上市,PCSK9抑制劑商業(yè)前景比較樂觀
2015年6月11日 FDA專家組推薦安進(jìn)Repatha上市,PCSK9抑制劑商業(yè)前景比較樂觀已關(guān)閉評(píng)論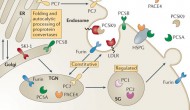
昨天FDA的分泌與代謝藥物顧問小組以13票贊成、3票反對(duì)的壓倒性結(jié)果支持賽諾菲的Praluent上市,今天幾乎是同一班人馬又以大致相同的投票結(jié)果(11票贊成、4票反對(duì))支持安進(jìn)的PCSK9抑制劑Repatha上市,其中全票(15:0)支持用于治療家族性高血脂癥患者。
Continue reading …FDA專家組13:3支持PCSK9抑制劑Praluent上市,但開始適應(yīng)癥可能很小
2015年6月10日 FDA專家組13:3支持PCSK9抑制劑Praluent上市,但開始適應(yīng)癥可能很小已關(guān)閉評(píng)論
今天FDA專家組以13票贊成、3票反對(duì)的投票結(jié)果支持賽諾菲/再生元的PCSK9抑制劑Praluent上市,明天將討論安進(jìn)的同類藥物。雖然Praluent獲得壓倒性支持,但適用人群至少暫時(shí)不會(huì)太大。
Continue reading …


















 微信號(hào):美中藥源
微信號(hào):美中藥源