
在日前正在舉行的美國神經(jīng)學年會上Mitsubishi Tanabe公布了其ALS藥物Edaravone的一個三期臨床試驗結果。在標準療法基礎上加入Edaravone顯著改善ALS患者綜合功能指標ALSFRS-R(-5.0對-7.5),同時也改善運動、呼吸等局部功能。
Continue reading …
今天法國生物技術公司Genfit宣布其NASH藥物elafibranor的三期臨床RESOVLE-IT招募病人速度緩慢。早期病人招募速度尚可,但晚期病人入組進度低于預期。
Continue reading …
本周的《科學》雜志發(fā)表一篇題為《化學登月計劃》(A moonshot for chemistry)的文章,介紹伊利諾伊大學Martin Burke教授的一個宏偉計劃。
Continue reading …
今天谷歌旗下Verily宣布將與斯坦福、杜克大學合作開始一個為期四年、招募1萬志愿者的健康信息搜集、跟蹤試驗。這個叫做基線計劃(Baseline Project)試驗開始時將檢測志愿者的多種血液、體液、糞便的各種指標和基因信息,志愿者四年內將跟蹤檢測5次。
Continue reading …
今天英國生物技術公司Circassia宣布其免疫療法、多肽抗原混合物在一個治療塵螨過敏的二期臨床失敗,Circassia將放棄這個技術平臺而專注于從阿斯列康收購的哮喘藥物開發(fā)推廣。
Continue reading …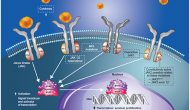
今天禮來/Incyte宣布他們的風濕性關節(jié)炎藥物、JAK1/JAK2雙抑制劑baricitinib的上市申請被FDA拒絕。FDA要求廠家證明最佳劑量,并要求提供更多安全性數(shù)據(jù)。
Continue reading …
今天施貴寶宣布將其Tau抗體BMS986168以3億首付、4.1億里程金轉讓給百健,同時將杜氏營養(yǎng)肌不良癥(DMD)藥物BMS986089以1.7億首付、2.1億里程金轉讓給羅氏。
Continue reading …
今天FDA批準了Neurocrine Biosciences的單氨轉運酶抑制劑valbenazine(商品名Ingrezza)用于治療成人遲發(fā)性運動障礙(TD)。TD是精神分裂藥物常見的副作用,15-30%使用精神類藥物患者會有這個副作用,也有少數(shù)人有原發(fā)TD。
Continue reading …
正在進行的AACR年會上報道了一些免疫療法的長期生存數(shù)據(jù),顯示一小部分幸運病人即使得了晚期腫瘤也可能被免疫療法接近治愈。比如晚期非小細胞肺癌使用施貴寶的PD-1抗體Opdivo五年存活率達到16%,而免疫療法之前的生存率低于5%。晚期惡黑患者使用Opdivo/CTLA4抗體Yervoy組合兩年存活率達到64%,雖然副作用也較為嚴重。Kite的CAR-T療法在晚期淋巴瘤也顯示持久的應答。
Continue reading …
今天默沙東和Incyte宣布將擴大二者在PD-1抗體Keytruda和IDO抑制劑Epacadostat的臨床合作。在此之前兩個公司已經(jīng)完成一個62人的一期臨床(ECHO-202)并開始了一個三期臨床
Continue reading …
昨天FDA批準了羅氏CD20抗體、多發(fā)性硬化癥(MS)藥物ocrelizumab 用于治療復發(fā)性(RRMS)和原發(fā)進展性(PPMS)硬化癥
Continue reading …
今天FDA批準了再生元/賽諾菲的IL-4/IL-13抗體dupilumab(商品名Dupixent)用于治療中重度濕疹。在三期臨床中Dupixent與激素聯(lián)用16周比單獨使用激素減少近30%(58%對29%)的嚴重皮膚瘙癢。
Continue reading …
今天FDA批準了Tesaro的PARP抑制劑niraparib(商品名Zejula)用于卵巢癌的維持療法。這是第三個上市的PARP抑制劑,此前阿斯利康的同類藥物Lynparza和Clovis的Rubraca已經(jīng)上市用于BRCA變異復發(fā)卵巢癌的治療。
Continue reading …
今天FDA批準了輝瑞和德國默克的PD-L1抗體avelumab (商品名Bavencio)用于治療一種叫做默克細胞癌(MCC,與默克公司無關,英文是Merkel不是Merck)的罕見皮膚癌。
Continue reading …





















 微信號:美中藥源
微信號:美中藥源